在工业过程、实验室和生物中,酶的活性可以用光来远程控制。这需要将它们固定在纳米颗粒表面并用激光照射。近红外光可以穿透活体组织而不损害它。
纳米粒子吸收辐射的能量,并以热量或电子效应的形式释放出来,触发或增强酶的催化活性。这就形成了一个新的研究领域,即等离子体生物催化。
巴西
这项研究得到了
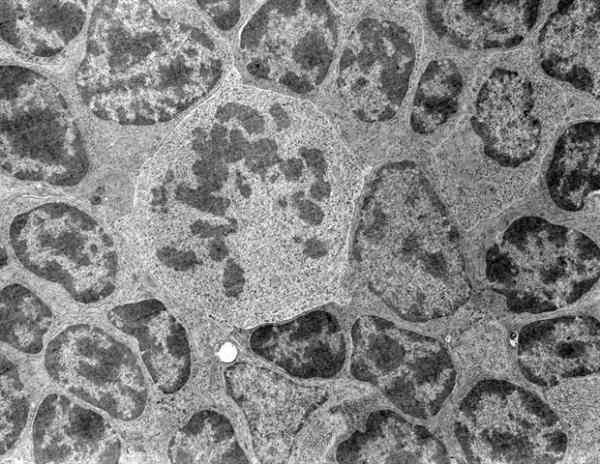
里贝罗·德·巴罗斯说:“我们用一种脂肪酶(CaLB)作为模型酶,将其固定在两种形状的金纳米颗粒上——球形和星形。”“红外激光仅通过外部光线照射就可以非侵入性地加速酶的活性。”
研究表明,纳米颗粒对酶的作用不仅受材料组成的影响,还受其几何形状的影响。
Ribeiro de Barros说:“当脂肪酶固定在金纳米星上时,酶的活性显著增强,增加了58%。”“相比之下,金纳米球促进了13%的小得多的增长。较大的增加对应于纳米星表面和激光辐射之间的共振效应。”
这里考虑的幅度是局域表面等离子体共振(LSPR)。纳米球的LSPR在525纳米处吸收,而纳米星的LSPR达到700 nm,更接近红外激光波长808 nm。
广泛的潜在应用包括加速工业规模化学反应的生物催化和致病酶的体内控制。在更遥远的未来,这种过程可能会被用于治疗帕金森病和阿尔茨海默病等疾病。当然,在它成为一种真正的替代品之前,还需要进行更多的研究。
“从医学的角度来看,这项研究的主要目的是指出在不久的将来治疗疾病的解决方案,而不需要侵入性手术,并通过特定的空间和时间方法来避免当前方法的副作用,”Ribeiro de Barros说。
点击分享到