在威尔康奈尔医学、纽约基因组中心和多伦多玛格丽特公主癌症中心的研究人员领导的一项研究中,一项使科学家能够记录单个细胞中基因突变和基因活动模式的技术已经扩展到RNA剪接。
更好地了解这一过程中的畸变如何影响细胞的发育和行为,对于理解癌症和其他疾病至关重要。
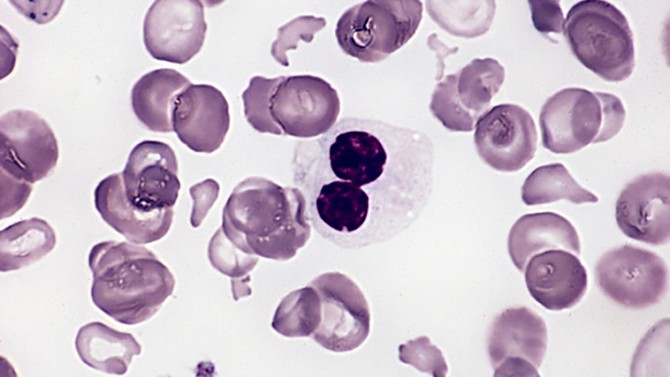
资料来源:美国武装部队病理研究所
骨髓增生异常综合征成年女性的血液涂片。
RNA剪接是指对活性基因的RNA转录本进行剪切和重组。RNA剪接是细胞中的一个基本过程,是在大多数基因的转录本上完成的,对于任何给定的基因,都可以产生几种不同的蛋白质,这些蛋白质至少具有细微的功能差异。在8月14日发表在《细胞干细胞》杂志上的这项研究中,研究人员修改了他们自己的一种细胞分析方法,使其也能产生RNA剪接的信息,从而使其对组织样本的详细分析变得实用。
研究小组利用这种新方法揭示了控制RNA剪接的基因突变是如何导致一种称为骨髓增生异常综合征(MDS)的血癌的。
“改变rna剪接过程的突变是许多癌症和其他疾病的基础,”该研究的资深作者Dan Landau博士说,他是威尔康奈尔医学院血液学和肿瘤医学部门的医学副教授,纽约基因组中心的核心教师和纽约长老会/威尔康奈尔医学中心的肿瘤学家。“这项工作使我们能够以前所未有的详细程度追踪这些变化的影响。”
该研究的共同第一作者是博士后研究员Mariela Cortés-López,生物信息学专家Paulina Chamely和博士后研究员Allegra Hawkins,他们都是研究期间的朗道实验室;以及纪念斯隆·凯特琳癌症中心的博士后罗伯特·斯坦利。
朗道和他的实验室研究癌症的起源和进化,以及可能导致癌症的前恶性状态。为了促进他们的研究,他们一直在开发新的“单细胞多组学”技术,这种技术可以分析单个细胞中的多层信息。单细胞技术避免了分析大量细胞混合物的传统方法的局限性。
2019年,Landau及其同事开发了一种称为转录组基因分型(GoT)的技术,首次实现了对单个细胞中基因突变和基因表达模式的高通量分析。在这项新研究中,研究小组修改了用于GoT的RNA测序方法,以便RNA剪接信息也可以从中得到。研究人员还整合了一种单独的方法,用于检测单个细胞上的蛋白质表面标记物。由此产生的“get - splice”技术可以记录来自单个细胞的四层不同的信息。
研究人员通过使用GoT-Splice来研究一种MDS的形式,证明了它的潜力,在这种MDS中,患者的骨髓细胞通常含有SF3B1的突变,SF3B1是一种在RNA剪接过程中起核心作用的基因。这种MDS患者的功能性红细胞水平较低,骨髓中存在大量未成熟红细胞,具有特征性异常。
利用GoT-Splice,研究小组分析了数以万计的患者细胞,详细描述了参与细胞存活、细胞成熟和其他关键过程的基因中的异常RNA剪接事件,并展示了这些影响在不同亚型的未成熟血细胞中是如何变化的。这些发现阐明了SF3B1突变(发生在干细胞样骨髓细胞中)如何使成熟过程向红细胞而非白细胞倾斜,导致MDS中未成熟红细胞的特征性异常,并允许含有突变的细胞增殖并比其他情况下存活更长时间。
“GoT-Splice使我们第一次将SF3B1突变与MDS患者未成熟红细胞中观察到的特定变化直接联系起来,”该研究的共同资深作者Federico Gaiti说,他是朗道实验室的博士后研究员,现在是多伦多玛格丽特公主癌症中心的助理教授。
研究人员发现,正常rna剪接被SF3B1突变破坏的基因之一是BAX,这是一种称为细胞凋亡的关键抗癌机制的中介,强调了这些发现的临床相关性。BAX突变先前与一些白血病患者对venetoclax药物产生耐药性有关。
利用GoT-Splice,研究人员还在无症状的克隆造血(CH)患者的骨髓细胞中发现了类似mds的变化——一种血细胞类型的轻度异常增殖——在这种情况下涉及SF3B1突变。
“在CH患者身上的发现表明,CH和显性疾病之间的联系更多是定量的,而不是定性的——如果异常细胞的克隆相对较小,那么其余的骨髓可以弥补,”Landau说,他也是威尔康奈尔医学院桑德拉和爱德华迈耶癌症中心的成员。
他和他的团队计划继续使用GoT-Splice作为揭示基因突变如何导致疾病细节的多功能工具。
许多威尔康奈尔医学院的医生和科学家与外部组织保持关系和合作,以促进科学创新并提供专家指导。该机构将这些信息公开,以确保透明度。有关此信息,请参阅Landau的配置文件。
吉姆·施纳贝尔是威尔·康奈尔医学公司的自由撰稿人。
/公开发布。来自原始组织/作者的材料可能具有时点性质,并根据清晰度,风格和长度进行了编辑。海市蜃楼。新闻不受机构限制
所有的位置或侧面,以及所有的视图、位置等
此处表达的结论仅代表作者的观点。点击此处查看全文。
<
点击分享到









