质膜修复缺陷可导致人类肌肉和心脏疾病。三方基序蛋白(TRIM)72 (mitsugumin 53);已经确定MG53在膜损伤部位快速成核囊泡,但其潜在的分子机制仍然知之甚少。在这里,我们提出了小家鼠TRIM72的结构,一个完整的模型的TRIM E3泛素连接酶。我们证明TRIM72与磷脂酰丝氨酸富集膜之间的相互作用是其寡聚物组装和泛素化活性所必需的。利用低温电子断层扫描和亚断层扫描平均,我们阐明了磷脂双层上TRIM72组装的高阶模型。结合结构和生化技术,我们开发了TRIM72的工作分子模型,为通过高阶组装中的多个结构域的合作调控ring型E3连接酶提供了见解。我们的发现为TRIM E3连接酶的研究奠定了基础,并对与膜修复相关的疾病具有治疗意义。
细胞需要修复质膜损伤以保护细胞质免受外界环境的影响。在肌肉组织中,质膜损伤经常发生在机械和代谢应激的反应中。幸运的是,膜修复机制可以迅速重新密封受损的质膜。膜修复缺陷可引起疾病,包括肌肉萎缩症和神经退行性疾病4,5,6。自最初发现膜重封7以来,已经提出了几种膜修复模型:补片、收缩、胞吐-内吞介导和运输所需的内体分选复合物(ESCRT)介导模型8,9。然而,尽管近年来从这些模型中获得了越来越多的生物学和生化理解10,11,12,13,14,15,但由于缺乏结构证据,很难阐明膜重封的分子机制。
一个关键因素是细胞外Ca2+内流通过Ca2+依赖的ESCRT系统和Ca2+诱导的溶酶体胞外分泌,在富含磷脂酰丝氨酸(PS)的受损部位触发膜修复2,16。然而,尽管Ca2+内流的重要性,还有一个独特的Ca2+独立的膜修复过程,已知是由三方基元蛋白(TRIM)72介导的(参考文献18)。TRIM72,也被称为MG53,在肌肉中高表达18,19,是促进囊泡运输到损伤部位的质膜修复机制的关键启动物18。此外,TRIM72在缺血再灌注损伤20和急性肾、肺损伤后的伤口愈合中具有保护作用21,22。它已被证明对肌肉和非肌肉组织的各种损伤具有治疗潜力23。除了参与膜修复过程外,TRIM72还具有与先天免疫应答24、胰岛素抵抗25、26和肌肉分化19相关的功能。然而,由于缺乏结构和生化方面的研究,其分子机制在很大程度上仍然是未知的。
TRIM72是TRIM超家族27的成员,TRIM超家族是真正有趣的新基因(RING)型E3泛素(Ub)连接的一个主要亚家族28。泛素化是一种关键的蛋白质质量控制系统,在该系统中,Ub通过E1、E2和E3酶级联催化的反应附着在底物上,导致底物被26S蛋白酶体降解。此外,已知Ub连接酶可触发信号转导、膜运输和DNA损伤修复过程29。根据其Ub转移机制将其分为三种类型:RING,同源E6AP C-Terminus (HECT)和RING-between-RING (RBR)连接30。RING型连接酶最为丰富,在人类600个Ub连接酶中,TRIM RING连接酶包含70多个成员31,32。TRIMs具有多模结构域的特征,包括保守的ring -b -box -coil -coil (RBCC)结构域和可变的c端结构域。虽然它们的结构域结构相似,但它们的功能和相关疾病,如抗病毒防御、癌症和遗传性疾病,都非常广泛32,33,34。然而,尽管有生物学证据,但由于TRIMs的灵活性和复杂性,对其进行深入的结构和生化研究相当有限35,36,37,38,39,40,41,42,43,44,45,45,46,47,48,49,50,51,52。
在这里,我们利用综合结构技术阐明了TRIM72的结构以及TRIM72与磷脂膜络合的高阶组装体。这些结构使我们能够了解TRIM72如何识别膜修复过程中独立于Ca2+的带负电荷的磷脂结构域。我们已经证明TRIM72与磷脂膜的结合诱导其自组装,从而通过分子间环结构域二聚化增强其泛素化活性。总之,我们提出了一种高阶TRIM72组装在磷脂膜上转移Ub的激活机制。
TRIM72是TRIM蛋白IV类的成员,是11组TRIM蛋白中最大的亚型。其结构域组织包括一个RBCC结构域,随后是一个与splA激酶和红嘌呤受体(PRYSPRY)结构域中鉴定的SPRY结构域相关的PRY基序(图1a)53。TRIM72是一种紧密二聚体,通过尺寸排除色谱(SEC)和多角度光散射(SEC - mals;扩展数据图1a,b),通过SEC耦合小角x射线散射(SEC - saxs;扩展数据图1c-f)。为了获得高分辨率模型,生成、纯化和结晶了许多构建体;然而,他们中的大多数衍射很差。在引入点突变和缺失后,我们最终能够解决小鼠TRIM72的分子模型,包括ring缺失(ΔRING, 2.75 ?;最高分辨率在括号中),全长(FL, 4.6 ?)和野生型(WT, 7.1 ?) TRIM72。所使用的构造和晶体结构的详细信息见补充表1和表1。
图1 TRIM72的晶体结构。
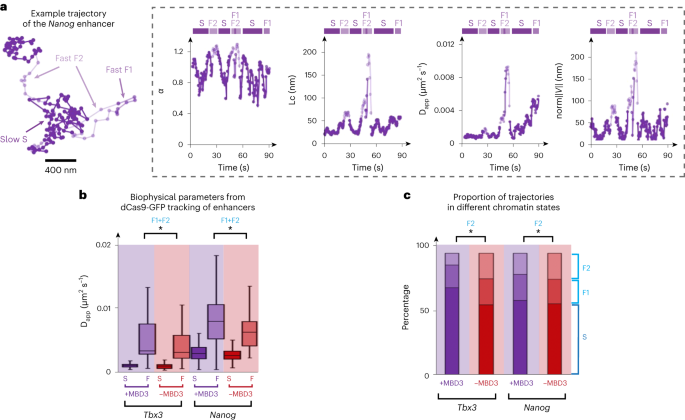
a、TRIM72的域组织。每个域和小motif如下图所示:RING(绿色);L1连接器,b盒(橙色);H1螺旋(粉色);helix-turn-helix, H2 helix(青色);L2连接器(薄荷);H3螺旋(黄色);和PRYSPRY(洋红色)。根据小鼠TRIM72序列对残基进行编号。b、小鼠TRIM72的整体结构,用带带状图的曲面模型表示。每个域的颜色对应于a中的域架构。第二个原聚体被标记为素数符号('),并以不太鲜艳的颜色显示。除RING结构域(绿色)来自TRIM72 FL (4.6 ?)外,其余结构模型均来自小鼠TRIM72 ΔRING (2.75 ?)。
表1 x射线晶体学数据收集和结构细化统计
TRIM72二聚体的整体结构呈细长形状(图1b和补充图1)。线圈结构域(CCDs)形成了长度约为17 nm的反平行二聚体的主支架(补充图2a-e)。在ccd的中间,结构核心由H1:H1 '螺旋('表示二聚体的第二个原聚体)和H3:H3 '螺旋组成,后面是一对PRYSPRY结构域(补充图2f)。在H1:H1 '螺旋和PRYSPRY结构域之间,H3:H3 '螺旋夹在中间,与这两个结构域相互作用。H3:H3 '螺旋的一侧与后十轴H1:H1 '螺旋包裹在一个四螺旋束中,另一侧通过疏水界面、氢键和离子相互作用与PRYSPRY的β-片接触(补充图2g,h)。由于这些结构域间的相互作用,两个PRYSPRY结构域横跨H3:H3 '螺旋位于ccd的另一侧(图1b)。
在N端,一个催化环以弯曲构象存在于CCD的另一个原聚物附近(补充图3a)。在RING结构域旁边,B-box结构域位于ccd的两端,并以疏水的方式接触ccd的H1和H2 '螺旋(补充图3b)。TRIM72的整体结构获得了TRIM家族成员的完整模型,使我们能够详细研究结构-功能关系。
PRYSPRY由两个反平行的β片组成:一个β片(β3、β5 -β8和β12)形成凹表面,另一个β片(β1、β2、β4、β9 -β11和β13)形成凸表面(图2a)37。TRIM72二聚体包含两个具有独特结构特征的PRYSPRY结构域。首先,几个精氨酸(R356, R368, R369, R371和R386)和赖氨酸(K317, K330, K389, K398, K460和K462)位于凹表面,由可变环(VLs)组成,并贡献其正电荷(图2a和扩展数据图2)。其次,每个PRYSPRY结构域显示一个凹表面,朝向ccd的同一侧带正电荷(图2b)。最后,PRYSPRY对通过与H3:H3 '螺旋的相互作用严格保持其取向(图2b和补充图2g,h)。通过广泛的蛋白-脂质覆盖分析,发现TRIM72特异性识别带负电荷的磷脂,如PS和磷脂酰肌醇,但不识别磷脂酰胆碱、磷脂酰乙醇胺、氧化磷脂或鞘脂(扩展数据图3)。流式细胞术分析显示,TRIM72还与含有PS的脂质体(PS脂质体)相互作用,其对30 mol% PS的亲和力远高于10 mol% PS(图2c)。这表明TRIM72-PS结合需要聚集和带负电荷的磷脂结构域。
图2:TRIM72的膜结合需要一对PRYSPRY结构域。
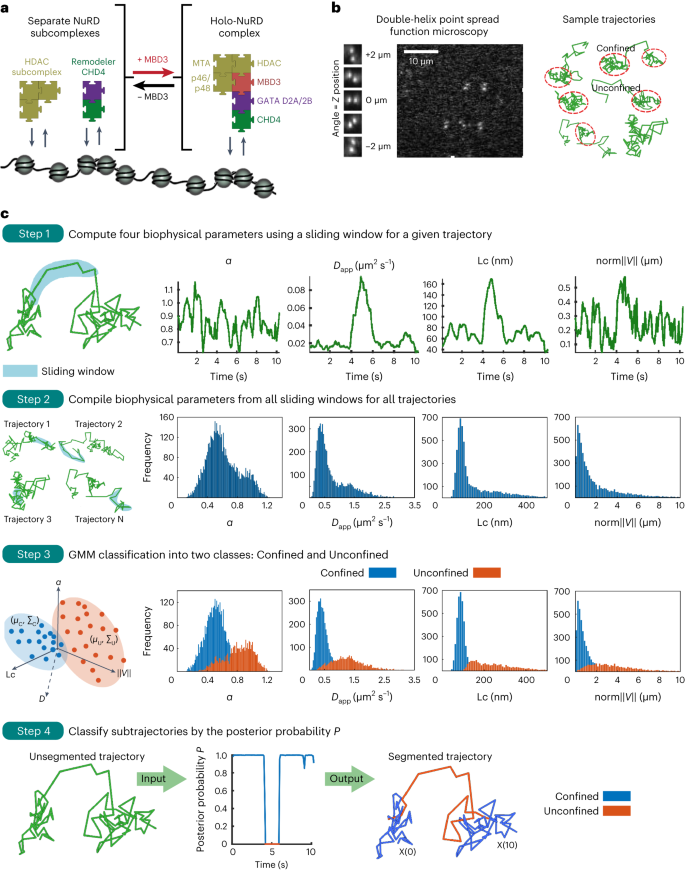
a, TRIM72的PRYSPRY结构域的带状结构。带正电的赖氨酸和精氨酸残基以棒状模型显示并标记。Ct指示羧基端。b, PRYSPRY畴的静电势面。每个PRYSPRY结构域的正电荷表面是由H3:H3 '螺旋(黄色)之间的相互作用维持的。第二个原聚体用素数符号(')标记。c,在PS浓度为30 mol%(红色)和10 mol%(蓝色)时,TRIM72与PS脂质体(lipo)结合的饱和曲线。d,使用蔗糖密度梯度对TRIM72 WT和突变体进行脂质体共浮试验。在试管中收集的馏分从上到下表示。用抗TRIM72抗体检测TRIM72。PC,含磷脂酰胆碱脂质体;PS, PS脂质体(30 mol% PS)。WB, western blot。X和O分别表示非绑定和绑定。e, TRIM72在C2C12成肌细胞中的亚细胞分离。显示了膜(Mem)和细胞质(Cyto)组分。实验方案(上图)由BioRender.com创建。Western blot结果见补充图4。独立实验一式三次。数据以平均值表示,误差条表示标准差。实验中使用的突变体的详细信息见补充表1。
源数据
为了研究PRYSPRY结构域与带负电荷的磷脂结构域之间的相互作用,我们使用TRIM72突变体K2D (K460D, K462D)和R3E (R368E, R369E, R371E)进行了脂质体共浮实验,这两个突变体在PRYSPRY结构域中引入了电荷反转。与WT相比,电荷反转突变体没有表现出与PS脂质体的任何相互作用(图2d)。我们还通过生成TRIM72突变体ΔH3(删除残基272-281)来检测PRYSPRY结构域相对于膜的方向,该突变体破坏了PRYSPRY结构域的方向。正如预期的那样,我们观察到PS脂质体和缺失突变体之间失去了相互作用,证实了PRYSPRY结构域的取向在识别带负电荷的磷脂膜中的重要性(图2)。接下来,我们测量了TRIM72与PS脂质体之间的结合亲和力。计算得到的结合常数KD为9.9 nM,与膜联蛋白V与PS的亲和力相似(扩展数据图4a,b)54。我们观察到二聚体谷胱甘肽s -转移酶(GST)融合的H3-PRYSPRY与PS脂质体相互作用的KD为76.7 nM,比WT低7.7倍(扩展数据图4a,g)。然而,与有缺陷的突变体RBCC、K2D、R3E和ΔH3相似,与MBP融合的单聚麦芽糖结合蛋白H3-PRYSPRY不与PS脂体结合(扩展数据图4)。因此,我们将这一结果解释为亲和力对TRIM72识别PS至关重要。
转染表达人TRIM72的C2C12成肌细胞,分离膜和胞浆,在体内也证实了这一结果。与TRIM72 WT相比,突变体(K2D、R3E和ΔH3)在膜定位上存在显著缺陷(图2e和补充图4)。因此,在生理条件下,TRIM72利用其带正电的PRYSPRY结构域与脂质膜结合。总之,我们的结果证明了PRYSPRY结构域的取向、亲和度和电荷分布在识别带负电荷的磷脂结构域中的重要性。
TRIM72已知以氧化依赖的方式寡聚,并且对于囊泡成核促进快速膜修复至关重要18。在添加H2O2氧化条件下,仅在PS脂质体中观察到寡聚的TRIM72(补充图5a)。这一结果表明TRIM72在带负电荷的磷脂膜上自寡聚。为了进一步表征TRIM72的多聚性,我们在PS脂质体存在或不存在的情况下,用各种巯基和胺反应性交联剂处理TRIM72(补充图5b)。在与PS脂质体结合的条件下,观察到高阶TRIM72低聚物。时间过程交联分析表明,随着时间的推移,TRIM72 WT逐渐寡聚,但突变体(K2D, R3E和ΔH3)产生的高阶低聚物较少,因为它们无法结合带负电荷的PS脂质体(扩展数据图5)。这些发现表明,TRIM72结合带负电荷的磷脂膜,然后寡聚成高阶组装体。
有趣的是,从哺乳动物细胞中纯化的人TRIM72交联速度比从细菌细胞中纯化的小鼠TRIM72快得多,这可能是由于其事先与哺乳动物细胞的内源性膜结合(扩展数据图6a)。事实上,在亲和层析(AC)和SEC中,哺乳动物表达的人TRIM72被直径约为100 nm的微泡共化(扩展数据图6b,c)。这些微泡被鉴定为起源于细胞外囊泡或连接膜,并富含TRIM72和Na+ -K + atp酶(补充数据1)。当微泡在阴性染色后通过透射电子显微镜(TEM)观察时,在微泡上观察到长条纹图案(扩展数据图6c)。为了确认这些图案是否来源于TRIM72寡聚体,我们在体外重组了TRIM72蛋白脂质体并对其进行了表征。TRIM72蛋白脂质体与TRIM72和直径约100 nm的小PS脂质体一起孵育后,通过SEC成功分离出TRIM72蛋白脂质体,并显示出与哺乳动物细胞中TRIM72结合的微泡相似的SEC特征(扩展数据图6b)。在负染色的TEM图像中,在重组的蛋白脂质体上也观察到长条纹模式,这与在微泡上发现的相似(扩展数据图6d)。
为了研究TRIM72如何在磷脂膜上寡聚,我们使用低温电子断层扫描(cro - et)分析了TRIM72蛋白脂质体(扩展数据图6e和补充视频1和2)。我们在脂质双分子层的两个表面观察到高阶TRIM72组装,内表面比外表面分辨率更高。TRIM72组件呈现出垂直柱状密度,以规则的间隔站立在脂膜上,并以独特的桥状结构水平连接这些柱状密度。
为了获得TRIM72在磷脂膜上组装的详细模型,我们从TRIM72蛋白脂质体的断层图中平均了含有TRIM72重复单元的亚断层图。这使我们能够以25 ?的总分辨率生成高阶TRIM72组装体与脂质双分子层配合的密度图(图3a,b,扩展数据图7和表2)。TRIM72组装体在脂质双分子层上以6 nm间距的规则模式出现,由垂直柱密度和跨越它们之间区域的平面密度组成(图3c和扩展数据图8c)。双柱密度连接脂质双分子层上方的平面密度,形成TRIM72组件特有的桥状结构。从垂直于脂质表面的角度详细观察了这种结构(图3b,c)。
图3:高阶TRIM72在脂质双分子层上的组装。
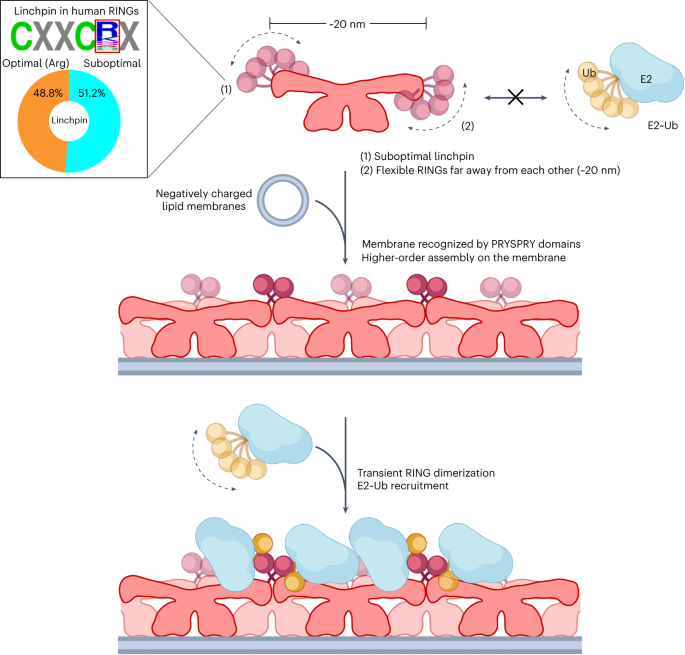
a,重组TRIM72蛋白脂质体的Cryo-ET图谱。俯视图(左)和前视图(右)为子层析图平均重建密度在1 σ等值线。b,脂质双分子层上的高阶trim72组装模型。左上为trim72组装模型的前视图(垂直于脂质表面),具有1 σ等高线的子层析图平均图。右上方,黑盒子在前视图被放大到一个特写视图。TRIM72组装的顶视图(与脂质表面平行,左下)和切片视图(右下)。顶视图中的黑框表示为d、e中的色带图。二聚体中突出显示的TRIM72原体分别为红色和蓝色。脂质双分子层模型以绿色棒状表示(右上)。TRIM72组装体和脂质双分子层的亚断层图平均重建图分别用白色和粉红色表示。c,在亚层析图平均重建中观察到的TRIM72的组装模式。z片的平均值对应于b中的中视图和前视图。y轴对应的相对强度(右;红色)和x轴(底部;蓝色)由前视图的平均z片计算得出。斜体数字(1-5)表示PRYSPRY域对应的柱状密度。请注意,PRYSPRY密度之间的规则间隔为6 nm(底部)。黑色刻度条,ac - c 5 nm。d、b盒之间的接口。相互作用残基和锌离子分别以棒状和球形模型表示。e, ccd中H1螺旋之间的界面。f,有或没有PS脂质体的TRIM72交联半胱氨酸残基的圆形图。经常识别的交联对用粗线表示。同型半胱氨酸桥接对显示为红色,并在PS脂质体的存在下被识别。g, TRIM72 WT及其突变体的脂质体共沉淀法。实验方案如图所示;该图像是用BioRender.com创建的。PC脂质体,含磷脂酰胆碱脂质体;颗粒图像的基本单位;吃晚饭,浮层。
源数据
表2 Cryo-ET数据收集
利用x射线晶体学和亚断层扫描平均,我们研究了高阶TRIM72与磷脂双分子层络合的分子结构。在晶体填充的指导下,我们能够将大约18个TRIM72二聚体作为刚体安装在大约1,400 nm2的磷脂双层上(图3b)。PRYSPRY结构域位于双柱状密度上,而其他结构域,如ccd、b -box和RINGs,则位于脂质双分子层上方的平面密度上。该组装允许PRYSPRY结构域的正电荷表面靠近磷脂双分子层的表面(图3b)。
TRIM组装中的每个二聚体之间有两个相互作用。主要的相互作用是b -box之间的相互作用,通过Gly106和Ser110 '通过氢键相互作用介导二聚体的形成(图3b,d和补充图6a,b)。通过交联质谱(CLMS)证实了这种相互作用,其中b -box (Cys105 -(交联剂)- Cys105 '和Cys105 -(交联剂)- cys108 ')之间的交联残基仅在PS脂质体存在时才被检测到(图3f和补充图7a)。B-box界面(TRIM72G106R和TRIM72S110R)的突变导致膜结合和组装缺陷(图3g)。
ccd介导的相互作用在确保PRYSPRY结构域在相同方向上排列方面也起着至关重要的作用(图3b,e)。这些CCD相互作用是由Met138介导的疏水界面组织的,Met138暴露在CCD H1螺旋的外侧。Met138位点(TRIM72M138A)的突变导致PS脂质体上高阶TRIM72组装的严重缺陷,尽管维持了膜结合(扩展数据图8a,b)。然而,与TRIM72 WT相比,TRIM72M138R变体对PS脂质体具有更高的结合亲和力,并且TRIM72的组装模式更清晰(扩展数据图8c和补充视频3和4)。对TRIM72M138R进行亚层析图平均显示,TRIM72M138R组装的密度图与TRIM72 WT相似(扩展数据图8d-g)。此外,在ccd之间的界面附近检测到交联残基(Cys144 -(交联剂)- Cys144 '),支持ccd之间接近性的观察(图3f和补充图7a)。
CLMS鉴定的交联半胱氨酸之间的距离用于验证高阶TRIM72组装模型。TRIM72组装模型显示交联半胱氨酸之间的距离最小,而二聚体或二聚体的二聚体模型显示50以上的异常值?(补充图7b和补充数据2)。总之,通过整合结构和生化分析,我们确定了高阶TRIM72组装与带负电荷的磷脂双分子层配合的分子模型。TRIM72组装在磷脂膜表面排列PRYSPRY结构域。此外,分子间结构域相互作用协同影响TRIM72的组装,以保持与带负电荷的磷脂膜更紧密的结合。
E2偶联酶的筛选显示TRIM72具有泛素化活性,与泛素偶联酶E2D (UBE2D)酶(补充图8a)结合。然而,与在哺乳动物细胞中表达的TRIM72(补充图8a)相比,在细菌细胞中表达的TRIM72,即使具有重复的RING结构域(2×RING),也没有表现出可检测的泛素化活性(补充图8b)。我们还检查了这些TRIM72蛋白的磷酸化状态,但没有发现它们之间的差异(补充图8c)。因此,我们研究了TRIM72的泛素化活性是否可以通过磷脂膜结合而增强。我们重组了TRIM72蛋白脂质体并评价了它们的泛素化活性。事实上,泛素化活性仅在重组的TRIM72蛋白脂质体中增加,而在单独的TRIM72或脂质体中没有增加(图4a)。这表明TRIM72的泛素化活性在溶液中受到抑制。为了研究泛素化活性是如何被抑制的,我们关注了最后一个锌配位半胱氨酸旁边的残基,称为“关键”。关键键对Ub转移至关重要,因为它与E2酶(UBE2Ds中的Gln92和UBE2N中的Lys94)和Ub (Arg72)的主链羰基氧原子形成氢键55,56。虽然典型的关键蛋白是精氨酸残基,但TRIM72中相应的残基是次优谷氨酰胺残基(Gln57)。我们将谷氨酰胺关键蛋白突变为精氨酸(Q57R),然后检测其泛素化活性。TRIM72Q57R突变体比TRIM72-WT蛋白表现出更高的泛素化活性(图4b)。膜结合的TRIM72Q57R突变体也比可溶性的TRIM72Q57R突变体表现出更高的泛素化活性,尽管可溶性TRIM72Q57R表现出部分恢复的泛素化活性。这些结果清楚地表明,在可溶性状态下,TRIM72的泛素化活性由于次优关键而受到抑制。与重组的蛋白脂质体类似,哺乳动物表达的TRIM72Q57R突变体在含有囊泡结合和囊泡无可溶性形式的两种组分中都具有高度增强的泛素化活性(补充图8d)。
图4 TRIM72的泛素化活性。
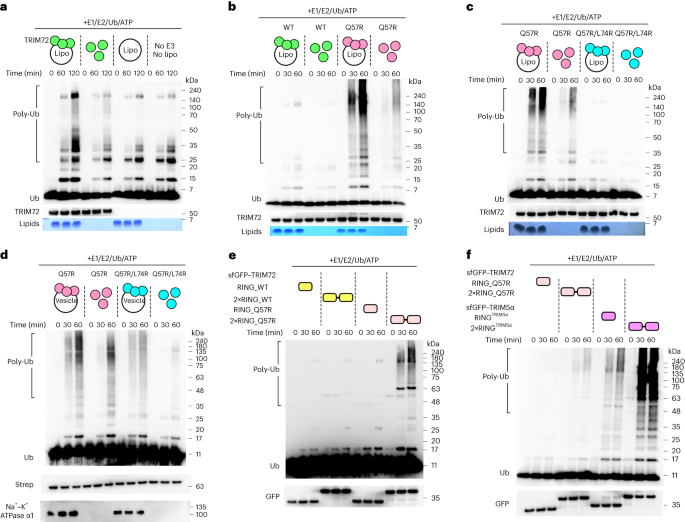
a,存在或不存在PS脂质体时TRIM72的泛素化活性。b,在PS脂质体存在或不存在的情况下,TRIM72Q57R泛素化活性增加。c,存在或不存在PS脂质体时TRIM72Q57R和TRIM72Q57R/L74R的泛素化活性。d, TRIM72Q57R和TRIM72Q57R/L74R内源性微囊结合或自由溶液状态的泛素化活性。e, trim72wt和TRIM72Q57R构建的RING和2×RING泛素化活性。f, TRIM72Q57R和TRIM5α构建的RING和2×RING泛素化活性。重组TRIM72蛋白脂质体,用SEC (a-c)进一步分离。从HEK293T细胞中纯化TRIM72微泡,并通过SEC分离(d)。Poly-Ub表示为多泛素化阶梯。接近140 kDa的条带被认为是泛素样修饰物激活酶1 (UBA1)~Ub。用抗Ub抗体检测Ub。分别使用抗strep -tag抗体或抗TRIM72抗体检测带有strep标记的TRIM72或完整的TRIM72 (a-d)。用抗gfp抗体检测绿色荧光蛋白(sfGFP)的超级文件夹变体-融合RING和2×RING结构(e,f)。磷脂用苏丹黑B (a-c)染色。用抗na + -K + atp酶α1抗体检测微囊泡(d)。TRIM72 WT,绿色;TRIM72Q57R,粉色;TRIM72Q57R / L74R,青色;TRIM72 RING_WT,黄色;TRIM72 RING_Q57R,浅粉色;TRIM5α环,洋红色。
源数据
在我们的TRIM72晶体结构中,通过弯曲的RING构象在CCD的Arg207 '附近观察到RING结构域的关键残基Gln57 (Supplementary Fig. 3a)。然而,当我们将该结构与TRIM25 RING - ube2d2 - ub三元配合物叠加43时,我们发现由于ccd的空间位阻,E2-Ub中间体无法接近弯曲的RING构象。为了进一步探索RING结构域的构象,我们通过灵活性(SREFLEX)方法对SAXS进行了细化(补充图9a-c;SAXS分析的统计数据汇总在补充表2)57中。基于实验SAXS剖面,计算模型显示RING区域具有高动态且不倾向于弯曲构象(补充图9a)。我们还观察到RING结构域的电子密度图只出现在TRIM72 FL的四种晶体结构中的一种,这表明RING结构域本质上是柔性的。此外,AlphaFold58预测表明TRIM72具有RING结构域的扩展构象,类似于SREFLEX计算的模型之一。不仅结构证据,而且生化数据表明,TRIM72Q57R和TRIM72Q57R/R207E突变体之间的泛素化活性没有差异(补充图9d)。因此,我们得出结论,RING结构域在磷脂膜上的TRIM72二聚体和低聚物中都具有高度的柔韧性。
接下来,我们研究了RING结构域的二聚化对Ub转移是否必要。与二聚体模型中的TRIM72 RING结构域相距约20 nm不同,在膜上的高阶组装模型中,RING结构域彼此靠近(图3b)。这表明TRIM72 RING结构域在二聚体TRIM72和低聚体中另一个二聚体TRIM72之间短暂二聚。为了确定RING结构域的二聚化是否对Ub转移至关重要,我们引入了一个突变来破坏RING结构域上的二聚体界面。与TRIM25环二聚体与UBE2D2-Ub43络合的结构比较,预测TRIM72的Leu74(对应TRIM25中的Val72)对RING结构域的二聚化至关重要。因此,我们将TRIM72的Leu74 (L74R)替换为大块的亲水性精氨酸残基来阻断二聚体界面。由于WT活性较弱,我们比较了TRIM72L74R与trim72q57r突变背景的泛素化活性。与高活性的TRIM72Q57R突变体相比,TRIM72Q57R/L74R在膜结合和可溶性形式中完全缺乏活性(图4c)。此外,我们不仅在重组的TRIM72蛋白脂质体上观察到类似的结果,而且在与内源性微囊结合的哺乳动物表达的TRIM72上也观察到类似的结果(图4d),这表明TRIM72 RING结构域在膜上二聚化并在高阶组装中激活。最后,我们以TRIM72Q57R为背景,利用TRIM72 RING和2×RING进行泛素化实验,剖析了TRIM72在没有其他结构域相互作用的情况下RING结构域的二聚化效应。与TRIM72 RING和2×RING的低泛素化活性相反,如前所述,TRIM72 2×RING_Q57R与单体TRIM72 RING_Q57R相比,其活性显著增加(图4e)。这一发现与TRIM5α RING的二聚体激活模式相似,尽管TRIM72 2×RING_Q57R的活性仍然低于TRIM5α RING(图4f)。这些结果表明,RING二聚化对于激活TRIM E3 Ub连接酶的机制是必要的。因此,我们得出结论,分子间环结构域可以在磷脂膜上的高阶TRIM72组装中瞬间二聚化以进行Ub转移。
除了其泛素化活性外,我们还研究了Ca2+对TRIM72和PS之间相互作用的影响。蛋白质-脂质覆盖分析显示,Ca2+抑制了TRIM72和PS之间的相互作用(图5a和扩展数据图3)。然而,这种相互作用被Ca2+螯合剂乙烯-二(氧乙烯腈)四乙酸(EGTA)完全恢复(图5a)。表明Ca2+直接抑制了TRIM72和PS之间的相互作用。我们的结构和生化证据表明,TRIM72和Ca2+的正电荷PRYSPRY结构域通过离子相互作用与带负电荷的PS头基竞争。这一发现与之前的报道部分冲突,即TRIM72以Ca2+不依赖的方式促进囊泡递送到受损部位18。我们通过逐个添加每个因子来仔细评估Ca2+的抑制作用。实时流式细胞术分析表明,在Ca2+存在下,TRIM72不能与PS脂质体结合(图5b,c)。令人惊讶的是,在添加Ca2+后,预加载的TRIM72几乎不与PS脂质体分离。相比之下,在膜联蛋白中,一个带负电荷的环参与Ca2+介导的与PS59头群的相互作用。这表明寡聚化作为二级相互作用模式,加强了TRIM72与磷脂膜上富含ps结构域之间的相互作用。综上所述,膜表面的高阶TRIM72组装,而不是溶液中的二聚体形式,可以克服Ca2+内流,并像修复囊泡一样被招募到质膜的受损部位,以促进伤口愈合。
图5:Ca2 +TRIM72的膜结合。
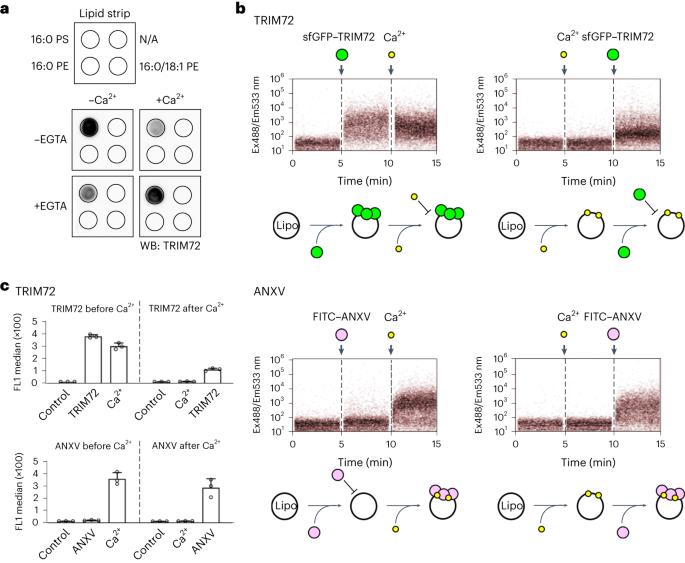
a,蛋白质-脂质覆盖分析显示干扰。TRIM72蛋白与脂质条孵育,存在或不存在Ca2+和/或EGTA,然后用抗TRIM72抗体进行探针检测。PE、磷脂酰乙醇胺。“N/A”表示不应用磷脂。b,流式细胞术分析比较Ca2+对TRIM72和膜联蛋白V (ANXV)的影响。将PS脂质体预先装载Ca2+或在Ca2+暴露后装载,然后与TRIM72或膜联蛋白v孵育,使用荧光标记的sfGFP-TRIM72和荧光素异硫氰酸酯(FITC) -膜联蛋白v Ex488/Em533 nm检测结合,激发在488 nm/发射在533 nm。c, b中数据的量化。实验进行了三次。数据以平均值±s.d表示。PS脂质体中PS浓度为30 mol%。Ca2+离子,黄色;TRIM72,绿色;膜联蛋白V,粉色。
源数据
从

摘要。
主要
结果
讨论
方法
数据可用性
参考文献。
致谢。
作者信息
道德声明
同行评审
扩展数据
补充信息
源数据
# # # # #
在本研究中,我们展示了ring型E3连接酶TRIM72在磷脂膜上组装成功能性低聚物(图6)。我们的研究结果表明,TRIM72在溶液中的泛素化活性是次优的,活性构象是由膜上的高阶组装引起的。这一过程是由细胞内由PS提供的带负电磷脂膜与PRYSPRY结构域方向相同的带正电表面相互作用介导的。结果,二聚体TRIM72在膜上排列,并进一步自寡聚成高阶组装。高阶TRIM72组装的构象允许RING结构域瞬时同二聚化。最后,E2~Ub中间体(波浪表示共价硫酯键)可以被招募到膜上高阶TRIM72组装的二聚环中,以实现有效的Ub转移。
图6:提出的TRIM72在膜上活化的工作模型。

在溶液状态下(上),TRIM72(玫瑰金)不能招募E2~Ub(青色,黄色)缀合物进行Ub(黄色)转移。二聚体TRIM72和动态ub偶联E2酶的两端RING结构域(粉红色)的灵活性用带箭头的曲线虚线表示。虽然b盒和两端的ccd也在垂直方向上移动,但为了清晰起见,在这个模型中没有描述这一点。关键蛋白的氨基酸频率在黑线框中显示。在303个人类RING结构域序列中分析了位于Zn2+配位半胱氨酸后残基的关键子(补充数据3)。注意,约50%的RING结构域具有次优关键子,包括TRIM72(谷氨酰胺关键子)。图中为带负电荷的膜上的高阶TRIM72组装(中)和具有E2~Ub共轭物的活性态模型(下)。当二聚体TRIM72靶向含ps的囊泡或富含ps的质膜时,它主要通过PRYSPRY结构域与膜结合。接下来,高阶TRIM72组装由B-box-B-box和CCD-CCD之间的协同相互作用介导。在这个组装中,动态环结构域减少了运动,分子间形成环二聚体。组装中的下一层TRIM72低聚物以不太鲜艳的颜色显示。最后,功能三元配合物足够稳定,可以进行高效的Ub转移。模型是用BioRender.com创建的。
源数据
TRIM72二聚体不适合在溶液中与UBE2D~Ub中间体进行Ub转移的原因有两个。首先,RING结构域在TRIM72 (Gln57)中拥有一个次优关键,即谷氨酰胺。与最优的关键子相反,最优的关键子在一半的环型Ub连接中作为精氨酸保存55,并在人类癌症中发生突变(图6和补充数据3)60,61,次优的关键子不足以作为氢键供体刺激灵活的UBE2D~Ub或UBE2N~Ub中间体进入封闭构象,以实现强大的Ub转移56,62。我们发现,改变关键键为最优精氨酸显著提高TRIM72在膜上和溶液中的泛素化活性。这一发现表明TRIM72的RING结构域,由于次优的关键子,不足以结合UBE2D~Ub中间体的封闭构象。为了获得与E2~Ub的适当结合亲和性,必须对已知TRIM蛋白中的环进行二聚化43,49,63,64。然而,第二个原因是环被反平行的ccd分开,并以单体构象排列(43,49,63,64)。考虑到ColabFold65的结构预测和支持RING二聚体的实验证据,60种TRIMs (TRIM15、TRIM40、TRIM45和VI类TRIMs除外)中的大多数都有可能以类似的方式拥有二聚环(补充数据4)。因此,与相对多样化的关键机制相比,RING二聚化可能是TRIM家族中活性构象的更普遍的机制43,63,64,66。
我们强调了环二聚化在膜上高阶TRIM72组装中诱导的活性构象。TRIM72组装是由分子间B-box相互作用和CCD相互作用协同产生的,导致RING结构域彼此紧密定位,尽管在溶液中亲和力非常弱,但仍会进一步二聚化。与灵长类动物TRIM5α的高阶组装相比,它结合并限制人类免疫缺陷病毒衣壳67,68,在这两种TRIMs的组装过程中都发现了b -box介导的相互作用。此外,诱导RING二聚化所需的接近性是通过两个TRIMs中b盒之间的相互作用实现的。因此,TRIMs中b -box介导的功能激活组装可能是一个共同的过程。另一方面,与TRIM5α的六边形和五边形组装相反,TRIM72的桥状组装模式是由溶剂暴露的ccd疏水表面之间的相互作用介导的,这表明TRIM组装的结构特征可能会因目标分子及其相互作用而变化。除了TRIM72和TRIM5α,包括TRIM65在内的IV类TRIMs的一个子集,通过其PRYSPRY结构域与同源维甲酸诱导基因I (RIG-I)样受体的RNA解旋酶结构域之间的亲和力驱动结合,可能在柔性双链RNA (dsRNA)细丝上寡聚50。最近对TRIM72和TRIM72 ΔRING晶体结构的低温电子显微镜(EM)分析也表明,CCD末端是动态的69,70。这些结果表明,长TRIM ccd的柔韧性适合于识别弯曲的细胞结构,如磷脂膜和病毒衣壳,以及丝状结构,如dsRNA和DNA。目前的发现为TRIM蛋白的研究提供了概念基础。与其他TRIM PRYSPRY结构域相比,这些PRYSPRY结构域使用凹表面52来识别其相互作用的分子(扩展数据图2a-f),这些PRYSPRY结构域与它们的结合分子相互作用已经得到了很好的研究36,50,51,68。结合的关键残基位于VL1、VL3 -β6-VL4和VL6上(扩展数据图2g),这表明底物特异性是由VL区域周围的序列多样性决定的。与其他PRYSPRY结构域相比,TRIM72 PRYSPRY结构域在VL区域显示出更多分布的带正电残基,这有助于其独特的膜结合基本性质(图2a,b和扩展数据图2a)。
TRIM72与膜的相互作用涉及肌肉分化和膜修复过程中空间控制的泛素化活性。我们的研究结果表明,高阶TRIM72组装对于其膜修复功能至关重要,正如先前报道的肌肉损伤18。我们已经阐明了TRIM72寡聚化的分子基础,包括对Ca2+非依赖性PS结合的偏好,寡聚化的关键残基,高阶TRIM72组装的结构和E3连接酶活性的激活。在膜修复的背景下,ESCRT机制起着至关重要的作用,它与Ub信号传导密切相关3,8,9,14。根据我们的观察,我们推测自泛素化或靶底物的泛素化可能有助于膜修复过程3。然而,需要进一步的研究来了解泛素化和膜修复机制之间的联系。尽管TRIM家族蛋白的一些特征是独一无二的,或者只是其中的一个子集,但从目前对TRIM72的结构和生化研究中获得的广泛信息为ring型E3 Ub连接酶提供了广泛的见解。
通过PCR扩增出小鼠Trim72和人Trim72基因,分别克隆到细菌(修饰pMAL和pRSF)和哺乳动物(修饰pHM6)表达载体中。利用pcr诱变技术克隆了结构域缺失和点突变体。所有构建体(补充表1)均通过DNA测序验证。WT TRIM72和带有n端His6-MBP标签的突变体在大肠杆菌BL21(DE3)细胞中表达并纯化。流式细胞术分析用n端His6-sfGFP71标记的小鼠TRIM72进行表达和纯化。纯化GST-H3-PRYSPRY的方法如上所述37。用500 μM异丙基β-d-1-硫代半乳糖苷在OD600为0.7的条件下诱导细胞,用200 μM ZnCl2(取决于编码RING和B2-box结构域的DNA的存在)在18°C下培养18 h。用离子交换(IEX)纯化蛋白质,并用平衡的SEC缓冲液(50 mM Tris- hcl, pH 8.0, 300 mM NaCl和1 mM Tris(2-羧乙基)膦(TCEP))进行SEC纯化。采用柱上酶切法对n端MBP标签进行了裂解。用AC和IEX将裂解的MBP标记和烟草蚀刻病毒蛋白酶去除。通过圆二色性和热移实验验证了TRIM72 WT和突变蛋白的质量。人TRIM72 WT和带有n端2x链球菌标签的突变体(MASAWSHPQFEKGGGSAWSHPQFEKGS)经聚乙烯亚胺转染后在HEK293T哺乳动物细胞中表达。48 h后,用Dulbecco的磷酸盐缓冲盐水(DPBS)洗涤细胞,并在裂解缓冲液(50 mM Tris-HCl, pH 8.0, 150 mM NaCl和1 mM TCEP)中重悬。超声探针裂解后,离心(27,216g, 4°C, 1小时),上清液上到StrepTrap HP色谱柱(Cytiva, 28907548)。用Strep洗脱缓冲液(50 mM Tris-HCl, pH 8.0, 150 mM NaCl, 1 mM TCEP和2.5 mM d-desthiobiotin)洗脱蛋白,然后使用Superose 6 Increase 10/300 GL柱(Cytiva, 29091596)进行SEC。每个含有TRIM72的片段都经过泛素化实验和EM。恒河TRIM5α环和环结构的串联重复序列使用His6-sfGFP标签和IEX纯化。从Addgene (http://addgene.org)上获得编码UBA1 (human UBA1, Addgene, 34965)72和UBE2D3 (human UBE2D3, Addgene, 15784)73的质粒。E1和E2酶用一般的细菌表达方法纯化。Ub的制备方法如先前研究所述74。
小鼠TRIM72蛋白(5-10 mg ml?1)用结晶试剂和蛋白1:1的混合气相扩散法结晶。虽然在22°C的初始结晶屏幕上获得了许多晶体,但这些晶体大多是脆性的,并且衍射差,分辨率仅为7 ?。为了提高晶体质量和改变晶体的包装,我们通过改变表面可能暴露的残留物设计了许多结构。其中,通过结晶包含5个点突变的结构体,并省略n端6个氨基酸和c端7个氨基酸,获得了不同的晶体形式(补充表1)。事实上,原始单斜晶在高达3.5 ?的分辨率下显示出大大改善的衍射模式。经过弹性酶有限蛋白水解进一步优化后,小鼠TRIM72 ΔRING晶体在4°C下生长,衍射值高达2.75 ?。结晶条件为:0.8 M NaCl和8% (vol/vol)乙醇(WT, 7.1 ?;构造,最高分辨率);100 mM ms - naoh, pH 6.5, 200 mM MgCl2, 0.5% (wt/vol)聚乙烯吡啶烷酮k15和30% (wt/vol)季戊四醇丙氧酸酯(5/4 PO/OH)微播(FL, 4.6 ?);100 mM HEPES-NaOH, pH 7.5, 230 mM MgCl2, 100 mM CsCl和34.16% (wt/vol)季戊四醇乙氧基酸酯(3/4 EO/OH)与Al 's油(FL, 3.5 ?);100 mM HEPES-NaOH, pH 7.5, 250 mM MgCl2和37% (wt/vol) 5/4 PO/OH (FL/C242S, 5.2 ?);100 mM Tris-HCl, pH 8.5, 30% (vol/vol) PEG 400,微播(ΔRING, 2.75 ?);和100 mM Tris-HCl, pH 8.5和8% (vol/vol) PEG 8000 (ΔRING, 3.3 ?)。晶体在冷冻保护条件下在液氮中快速冷冻。数据集在以下同步加速器设施收集:韩国的浦项加速器实验室和日本的光子工厂和超级光子环-8 GeV (SPring-8)。数据处理、集成和缩放使用来自HKL-2000套件75的DENZO和SCALEPACK进行。表1总结了详细的统计数据。
小鼠TRIM72 ΔRING用分子置换法求解相。phaser76以human TRIM72 PRYSPRY (PDB 3KB5)为检索模型37。通过结合两个锌离子在B-box域中的单波长异常色散,改善了相。用Coot77手工建立B2-box域和CCD的未分配模型,并用phoenix进行重建。优化周期之间的自动构建其他晶体的物相通过分子置换求解,以ΔRING单体为搜索模型。表1总结了详细的细化统计信息。在FL小鼠TRIM72结构中,仅在FL的三角晶体中发现了与RING结构域对应的电子密度图,其衍射分辨率高达4.6 ?。在其他晶体体系中,我们找不到足够的环域电子密度;因此,我们认为在这些晶体体系中RING结构域不参与晶体接触,并且它也是非常动态的。RING结构域的电子密度图位于另一个原聚体CCD的外表面,并被两个大的差密度图分开。两个锌离子被放置在每个分离的差异图的中心。有趣的是,锌离子之间的距离约为14 ?,这是经典的c3hc4型RING结构域的锌间距离79。由于分辨率较低,我们首先使用SWISS-MODEL80通过同源建模建立RING域坐标,然后将模型拟合到残差图中,并使用phenix.refine81进行细化。最终模型的质量通过MolProbity82进行验证。
使用CCP4套件中的PISA服务器进行结构分析。使用PROMALS3D84进行基于结构的序列比对。序列与Clustal Omega85比对,并用BioEdit软件86进一步分析。logo图形是用WebLogo (https://weblogo.berkeley.edu/logo.cgi)生成的。使用PyMOL (Schr?dinger)和UCSF ChimeraX87制作结构图。
在SAXS缓冲液(25 mM Tris-HCl, pH 8.0, 300 mM NaCl, 1 mM TCEP和1 mM二硫苏糖醇(DTT))中制备纯化的小鼠TRIM72-WT和ΔRING蛋白。SAXS的数据是在韩国浦项加速器实验室的同步加速器4C和日本光子工厂的同步加速器10C上收集的。在SEC-SAXS实验中,蛋白质被加载到Superdex 200 Increase 10/300 GL树脂(Cytiva, 28990944)上,用SAXS缓冲液平衡,然后从峰分数和归一化缓冲分数中收集数据集进行背景减法。数据处理采用ATSAS软件包88。为了灵活地改进TRIM72-WT模型,将二聚体TRIM72 FL的两个RING结构域定义为单独的刚体,并使用ATSAS online中的SREFLEX软件拟合小鼠TRIM72 WT的实验曲线57。最终模型叠加在25个精化模型上。数据收集的细节和参数汇总在补充表2中。
SEC-MALS采用?KTA FPLC系统(Cytiva)与Wyatt miniDAWN TREOS检测器(Wyatt Technology)结合进行。蛋白上载于Superdex 200 Increase 10/300 GL柱,用MALS缓冲液(50 mM Tris-HCl, pH 8.0, 300 mM NaCl和2 mM TCEP)平衡。卵清蛋白(Sigma-Aldrich, A7641)作为各向同性散射体用于探测器的校准和归一化。采用Wyatt Technology公司的ASTRA V软件进行光散射测量和分析。
采用50 nM UBA1, 500 nM每种E2酶(Boston Biochem, K-980B), 10 μM UBA1, 2 μM小鼠TRIM72构建物,37°C泛素化缓冲液(50 mM Tris-HCl, pH 8.0, 150 mM NaCl和1 mM TCEP), 1 h进行E2体外筛选实验。用50 nM UBA1、2 μM UBE2D3和3 μM UBA1与1 μM小鼠TRIM72、恒河鼠TRIM5α或0.2 μM人TRIM72进行体外泛素化反应。在基于Q57R背景的TRIM72突变体泛素化实验中,用0.5 μM UBE2D3代替2 μM UBE2D3来评估TRIM72的突变效应。所有的反应都是由5mm ATP和MgCl2的加入引发的。加入含有β-巯基乙醇(β-ME)的十二烷基硫酸钠(SDS)样品缓冲液阻止反应。样品在95°C煮沸10分钟,然后通过SDS-PAGE进行进一步分析。多泛素化链采用ub特异性抗体P4D1 (Santa Cruz, sc-8017)或VU-1 (LifeSensors, VU101)进行western blot检测,TRIM72 WT和突变体采用兔多克隆抗TRIM72(残基90-277)抗体19进行检测,融合sfgfp的TRIM构建体采用小鼠单克隆抗gfp抗体(Santa Cruz, sc-9996)进行检测。磷脂用苏丹黑B染色(Sigma-Aldrich, 199664)。采用小鼠单克隆抗na + -K + atp酶α1抗体(Santa Cruz, sc-21712)检测trim72结合的微泡。
蛋白质-脂质覆盖试验的概念先前已经描述过89。使用以下脂质试纸筛选TRIM72的脂质特异性:PIP试纸(Thermo Fisher Scientific, P23750)、Inositol Snoopers (Sigma-Aldrich, 330500)、氧化磷脂Snoopers (Sigma-Aldrich, 330501)和磷脂Snoopers (Sigma-Aldrich, 330503)。脂质条用3% (wt/vol)牛血清白蛋白(BSA)阻断;A0100, GenDEPOT)在TBS-T (10 mM Tris-HCl, pH 7.4, 140 mM NaCl和0.1% (vol/vol)吐温-20)中室温(22℃)保存1小时。阻断后,用TBS-T洗涤5次,并与1 μg ml?1小鼠TRIM WT、3% (WT /vol) BSA和TBS-T在4°C下孵育过夜。为了确定Ca2+的影响,使用2.5 mM CaCl2和10 mM EGTA (Sigma-Aldrich, E3889)作为Ca2+螯合剂。采用兔多克隆抗trim72抗体19检测脂质结合特异性。
采用涡旋法和挤压法制备新鲜脂质体。化合物1,2-二油基-sn-甘油-3-磷酸胆碱(DOPC;Sigma-Aldrich, 850375C), 1,2-二磺酰基-sn-甘油-3-磷酸-l-丝氨酸(DOPS;Sigma-Aldrich, 840035C), 1,2-二棕榈酰基-sn-甘油-3-磷酸-l-丝氨酸(DPPS;将Sigma-Aldrich, 840037P)和胆固醇(Sigma-Aldrich, C8667)溶解在氯仿或氯仿-甲醇(2:1)溶液中。在高于相变温度的通风柜下,将含有所述组合物的一微摩尔脂在玻璃小瓶中蒸发。干燥的脂质膜通过涡流充分水化生成大脂质体。为了制备小脂质体,将水合脂质体在水浴中超声处理1小时,并使用Avanti Mini-Extruder (Sigma-Aldrich, 610005)通过0.1 μm聚碳酸酯膜(Sigma-Aldrich, 610005)挤压35次。采用DynaPro Titan动态光散射仪(Wyatt Technology)进行动态光散射,评估脂质体的质量和大小,然后进行EM。
采用超声和挤压法制备了100 mol% DOPC或30 mol% DPPS和70 mol% DOPC组成的小脂质体。小脂质体与7 μM小鼠TRIM72 WT和突变体蛋白在室温下孵育30 min。将脂质体-蛋白混合物转移到离心管中,然后按以下顺序将蔗糖溶液覆盖在混合物上:300 μl 68% (wt/vol)蔗糖,2.5 ml 17% (wt/vol)蔗糖和1 ml 6.8% (wt/vol)蔗糖在DPBS中。不连续蔗糖梯度在272,800g、4℃下离心3 h。从梯度顶部到底部的每个部分用SDS-PAGE分离,用兔多克隆抗trim72抗体(Abcam, ab154238)进行western blotting分析。
采用旋流法制备了DOPC和胆固醇含量分别为80 mol%和20 mol%或PS和20 mol%的大脂质体。将大脂质体与50 μg小鼠TRIM72 WT或各突变体室温孵育30 min。将脂质体-蛋白混合物在21,130g、4℃下离心10 min,然后分成上清和颗粒两部分。每个分馏样品用SDS-PAGE分离,考马斯氏染色检测信号。
荧光标记sfGFP-TRIM72 WT和fitc标记的annexin V (FITC-annexin V;BioLegend, 640945)制备用于流式细胞术分析。在FACS缓冲液(50 mM Tris-HCl, pH 8.0, 150 mM NaCl, 1 mM TCEP和0.5% (wt/vol) BSA)中超声制备荧光标记和新生脂质体。采用0.1 mol% 1,2-二油基-sn-甘油-3-磷酸乙醇胺- n-(丽胺罗丹明B磺酰基)标记含有99.9 mol% DOPC或30 mol% DPPS和69.9% DOPC的脂质体(Sigma-Aldrich, 810150P)。罗丹明标记脂质体使用Accuri C6流式细胞仪(BD Biosciences),以488 nm激发激光和533/30 nm (FL1;波长/滤光片)和585/40 nm (FL2)发射探测器。检测阈值设置为前向散射高度为2000,FL2高度为100。sfGFP(或FITC)和罗丹明之间的光谱重叠被sfGFP - trim72 - wt结合的无罗丹明30 mol% PS脂质体和无罗丹明标记的30 mol% PS脂质体补偿。为了分析Ca2+效应,实时流式细胞术通过以下三个连续步骤进行:(1)仅测量脂质体,(2)测量添加了蛋白(sfGFP-TRIM72 WT或FITC-annexin V)的脂质体,(3)测量添加了CaCl2(终浓度为2.5 mM)的脂质体和蛋白。每个步骤进行5分钟,使用BD Accuri C6 Plus软件(BD Biosciences)对数据进行评估。
表面等离子体共振数据采集采用Biacore T200仪器(Cytiva)和Series S传感器芯片L1 (Cytiva, 29104993)。通过超声和挤压法制备小脂质体用于固定化。将含有100 mol% DOPC的固定化小脂质体(参比流式细胞)的信号与含有30 mol% DPPS和70 mol% DOPC的固定化小脂质体(第二流式细胞)的信号相减,计算传感器图。为了提高固定化效率,将含有30 mol% PS和2.5 M NaCl溶液的脂质体1:1混合注入流动池。固定后,使用0.2 mg ml?1无脂肪酸BSA (Sigma-Aldrich, A7030)阻断两种脂质体样品以防止非特异性结合。归一化后,注射连续稀释的蛋白。传感器芯片的再生是通过在测量之间加入50 mM NaOH溶液进行的。结合动力学计算采用BIAevaluation (Cytiva)软件。
C2C12成肌细胞在DMEM培养基中培养,DMEM培养基中添加10% (vol/vol) FBS (Cytiva, SH30071.03IH25-40)、青霉素(100 IU ml - 1)和链霉素(100 μg ml - 1)。用Neon转染系统(Thermo Fisher Scientific, MPL5000)将编码2x Strep-human TRIM72 WT和突变体的质粒转染到细胞中。48 h后,收集细胞,使用memo - per Plus膜分离试剂盒(Thermo Fisher Scientific, 89842)将细胞分离成膜和胞浆两部分。每个分离样品(10 μg)通过SDS-PAGE进行分离,并使用以下抗体进行western blotting分析:抗strep (IBA, 2-1509-001),抗caveolin-1 (CST, 3238),抗gapdh (Santa Cruz, sc-47724)和抗β-actin (Santa Cruz, sc-47778)。
TRIM72-WT蛋白与由80 mol% DOPS和20 mol%胆固醇组成的小脂质体在室温下孵育3小时。使用Spin-X (Sigma-Aldrich, CLS8162)离心过滤后,在交联缓冲液中使用Superose 6 Increase 10/300 GL树脂进行SEC纯化TRIM72蛋白脂质体。纯化后的TRIM72蛋白脂质体在4℃下与150 μM的交联剂分别孵育90 min:双(马来酰亚胺)乙烷(BMOE);赛默飞世尔科学,22323),1,4-双马酰亚胺-二乙二醇(赛默飞世尔科学,22331),1,8-双马酰亚胺-二乙二醇(赛默飞世尔科学,22336),1,11-双马酰亚胺-三乙二醇(赛默飞世尔科学,22337),二(磺基琥珀酰亚胺基)戊二酸酯(ProteoChem, C1126)和二(磺基琥珀酰亚胺基)亚盐(赛默飞世尔科学,21580)。加入25 mM Tris-HCl, pH 7.5和25 mM DTT,用含有β-ME的SDS样品缓冲液在95℃煮沸5分钟,停止反应。用质谱法对交联产物进行分析。为了进行时间依赖性交联反应,将小鼠TRIM72 WT和突变体与含有100 mol% DOPC或30 mol% DPPS和70 mol% DOPC的DPBS小脂质体在室温下预孵育30分钟。在室温下,将20 μM BMOE加入到蛋白质-脂质体混合物中引发反应。在加入BMOE引发交联反应后,在每个时间点加入25 mM DTT并在95℃下用含有β-ME的SDS样品缓冲液煮沸5min停止交联反应。SDS-PAGE分离交联蛋白,考马斯氏染色检测信号。
从HEK293T细胞中纯化人TRIM72微泡。使用StrepTrap HP柱,通过AC将囊泡结合的自由溶液TRIM72共纯化,并通过SEC完全分离(详细信息请参见上面的克隆、蛋白表达和纯化部分)。为了获得小鼠TRIM72蛋白脂质体,通过超声和100 nm滤光器提取制备了组成为30 mol% DPPS和70 mol% DOPC的小脂质体。将小脂质体与纯化小鼠TRIM72- wt蛋白的混合物在室温下轻轻搅拌3小时,重建TRIM72蛋白脂质体。用SEC进一步分离小鼠TRIM72蛋白脂质体和游离小鼠TRIM72蛋白。避免使用洗涤剂以保持微泡或脂质体的结构。对于阴性EM,将含有TRIM72微泡或TRIM72蛋白脂质体的每个峰段加载到发光碳涂层网格(Electron Microscopy Sciences, CF200-Cu)上,然后用1% (wt/vol)醋酸铀酰进行冲洗和染色。使用200 kV的Tecnai F20显微镜(FEI),在电荷耦合器件相机(2k × 2k, Gatan)上记录负EM图像。
在冷冻et实验中,小鼠TRIM72蛋白脂质体与小鼠TRIM72 WT和含有80 mol% DOPS和20 mol%胆固醇的小脂质体孵育重组。重组的TRIM72蛋白脂质体进一步用低温et缓冲液(50 mM Tris-HCl, pH 8.0, 150 mM NaCl和1 mM TCEP)进行SEC纯化。将蛋白脂质体装入发光孔网(Quantifoil R1.2/1.3 300 Mesh, Copper;EMS, Q350CR1.3),然后使用Vitrobot Mark IV系统(Thermo Fisher Scientific)在4°C和90%相对湿度下进行玻璃化。倾斜系列图像在韩国基础科学研究所收集,使用Titan Krios G2 (Thermo Fisher Scientific)透射电子显微镜,使用Falcon 3EC直接电子探测器(Thermo Fisher Scientific),使用断层扫描4.0 (Thermo Fisher Scientific)软件,在300 kV下工作,倾斜范围为- 60°至60°,角度增量为2°。图像的离焦范围在- 4.0和- 6.0 μm之间,标称放大倍数为×47,000,对应于1.4 ?的像素尺寸。每次断层扫描的总剂量约为200e?/?2。使用IMOD package90进行倾斜序列对齐、对比度传递函数(CTF)校正和层析成像重建。层析图使用加权反投影(WBP)和类似于同步迭代重建技术(SIRT)的滤波器进行重建,并进行四次分类,像素大小为5.6 ?。
为了对小鼠TRIM72-WT和trim72m138r突变体的蛋白脂质体进行亚断层图平均,我们通过涡流制备了含有80 mol% DOPS和20 mol%胆固醇的大脂质体。将大脂质体与小鼠TRIM72 WT在4℃下孵育90 min。将大脂质体与TRIM72 WT的混合物在312,200g、4℃条件下进行蔗糖梯度离心,分离1h。收集含有TRIM72-WT蛋白脂质体的共浮组分,浓缩至0.1 mg ml?1。由于磷脂分子的光谱和比色干扰,通过与量化的TRIM72蛋白的波段强度比较,计算出TRIM72蛋白脂质体的蛋白浓度。采用脂质体共沉淀法制备TRIM72M138R蛋白脂质体。在水浴中超声1h制备大脂质体。将超声脂质体与TRIM72M138R蛋白的混合物在21,130g、4℃下离心10 min。去除上清后,将颗粒洗涤三次,并在冷冻et缓冲液中重悬。TRIM72-WT和TRIM72M138R蛋白脂质体被装载到发光孔网格上(Quantifoil R1.2/1.3 300 Mesh, Copper;EMS, Q350CR1.3),然后使用Vitrobot Mark IV系统在4°C和90%相对湿度下进行玻璃化。为了增强倾斜序列图像的对准性,使用AURION Gold Tracer (AURION, 210.133)作为基准标记。将10 nm大小的金-牛血清白蛋白纳米颗粒在离心后通过收集溶液的颗粒部分进行浓缩,然后在玻璃化程序之前以1:5 (vol/vol)的比例与样品混合。倾斜系列图像采集使用300 kV的Titan Krios G2显微镜,配备Falcon 3EC直接电子探测器,角度范围为?54°~ 54°,角度增量为3°。图像使用离焦在- 4.0和- 6.0 μm之间记录,标称放大倍数为×29,000,对应于像素尺寸为2.3 ?。每次断层扫描的总剂量约为52 e?/?2。倾斜序列使用基准标记对齐。利用SIRT和WBP重建层析图,像素分割为2倍,像素大小为4.6 ?。采用SIRT重建对子层图位置进行标注,采用WBP重建对子层图进行平均。
使用Dynamo package91从TRIM72-WT和TRIM72M138R蛋白脂质体重建层析图中提取粒子坐标。在分配粒子坐标时,根据蛋白脂质体的形状,应用囊泡或椭球囊泡模型。我们从TRIM72-WT和TRIM72M138R蛋白脂质体重建层析图中分别提取了18,715和6,379个粒子坐标。倾斜系列中的显微照片使用MotionCor2(参考文献92)进行波束诱导运动校正,然后使用CTFFIND4(参考文献93)进行CTF估计。使用RELION-4.0(参考文献94)导入子层析图坐标、层析图对齐信息和估计的CTF进行子层析图平均。从4个盒大小为96像素和裁剪盒大小为48像素的分箱伪子层析图中获得初始模型。通过一系列连续的步骤,对三维粒子进行定向分类、细化和不定向进一步分类。迭代细化执行,而显微照片逐步解盒到原始像素大小。在去除30个?以内的重复项后,对改进后的模型进行CTF细化和帧对齐,其中框大小为512像素,裁剪后的框大小为192像素。基于0.143的FSC,估计TRIM72-WT和TRIM72M138R蛋白脂质体重建的最终分辨率分别为25和26 ?。子层析图平均过程如图8a所示。表2总结了cryo-ET的统计数据。用Fiji95分析亚层图平均重建投影的相对强度。脂质双分子层上高阶TRIM72组装的初始模型来源于小鼠TRIM72的晶体包装ΔRING。我们使用UCSF ChimeraX87通过刚体拟合将初始模型与cryo-ET图对接。对拟合模型进行了进一步优化。Dock_in_map '(参考96)。采用CHARMM-GUI97计算脂质双分子层模型。
交联蛋白对应的每个条带用胰蛋白酶凝胶内酶切进行LC-MS /MS分析。LC-MS /MS分析采用Dionex UltiMate 3000纳米高效液相色谱系统与Q精确质谱仪(Thermo Fisher Scientific)在线耦合进行。色谱分离采用150-mm × 75-μm Acclaim PepMap C18反相分析柱(Dionex),梯度洗脱(溶剂a, 0.1%甲酸水溶液;溶剂B: 0.1%甲酸乙腈;0-10分钟,2% B;40分钟,30% B;44-49分钟,90% B;50-60 min, 2% B)。采用前10种数据依赖的MS/MS扫描方法获取MS数据。使用MSConvert将原始数据转换为MGF格式,并使用plink 2搜索包含小鼠TRIM72蛋白的数据库(参考文献98)。以1%的错误发现率过滤肽谱匹配。通过手工验证进一步确认交联肽的MS/MS谱。我们的结构模型中交联残基之间的距离是用Xwalk99计算的。
将从哺乳动物细胞中共纯化的含有TRIM72微泡的馏分溶于含有50 mM Tris-HCl, pH 8.0和4% (wt/vol) SDS的裂解缓冲液中,并加入蛋白酶抑制剂混合物。SDS裂解物用滤过辅助样品制备(FASP)消化,如前所述100。LC-MS /MS分析采用上述交联质谱法。ms衍生数据通过Proteome Discoverer平台(version 2.2.0.388, Thermo Fisher Scientific)在UniProt数据库中搜索人类条目。SEQUEST算法的搜索参数为:半胱氨酸氨基甲基化为固定修饰,甲硫氨酸氧化为可变修饰,前体质量公差为10 ppm,片段质量公差为0.02 Da。使用基于q值的渗透器验证肽谱匹配,错误发现率为1%。采用DAVID软件进行基因本体分析,评价生物功能101。P值< 0.05为差异有统计学意义。
有关研究设计的更多信息可在本文链接的自然组合报告摘要中获得。
ccDownload: /内容/ pdf / 10.1038 / s41594 - 023 - 01111 - 7. - pdf
点击分享到










