生物屏障严重制约了口服给药系统在疾病治疗中的有效反应。由于复杂的胃肠道环境要求载体具有不同甚至相互矛盾的特性,因此基于单一构造手段的载体很难同时克服这些障碍。有趣的是,孢子衣壳(SC)具有许多独特的生物学特性,如高抗性、良好的稳定性等。这为构建基于SC的无需进一步修饰的多功能口腔纳米平台提供了无限的灵感来源。在此,我们开发了一种仿生孢子纳米平台(SC@DS NPs),以先后克服口腔生物屏障。首先,多柔比星(DOX)和索拉非尼(SOR)自组装形成无载体纳米颗粒(DS NPs)。随后,SC有效地从益生菌孢子中分离出来,并作为递送DS NPs的功能载体。正如预期的那样,SC@DS NPs在口服后可以有效地通过崎岖的胃环境,并进一步运输到肠道。令人惊讶的是,我们发现SC@DS NPs在粘液渗透和经上皮运输方面表现出明显的改善,这与SC的蛋白种类有关。本研究表明SC@DS NPs可以有效地克服多种生物屏障,提高治疗效果。
胃肠道(GIT)是大多数口服药物传递和治疗干预的主要区域[1]。然而,GIT的多重生物屏障严重限制了口服纳米颗粒(NPs)在肠道疾病治疗中的有效反应[2,3]。考虑到胃肠道环境的复杂性,最佳的口服给药系统应稳定,以防止药物在胃中过早释放[4]。此外,递送系统还应有效地解决包括粘液和上皮屏障在内的关键障碍,这就要求载体具有不同甚至相互矛盾的特性[5,6]。例如,靠近电中性电荷的NPs表面有利于逃离黏液的包裹,但不利于上皮细胞的摄取,导致吸收和上皮间转运较差[7]。目前,已经有大量研究构建了多种药物传递载体,通过机械地结合一些特定的功能和部分来克服这些障碍[8,9,10]。然而,合成或修饰的载体在给药后复杂且不可控,这可能会阻碍NPs的进一步吸收效率。因此,开发一种简单稳定的口服给药纳米平台以克服上述难题是当前研究的重点。
最近,仿生策略在药物递送、生物材料设计和开发等各个领域都很流行,并取得了令人兴奋的进展[9,11,12,13,14]。有趣的是,在自然界中观察到的独特的保护机制,如植物种子休眠[15]和细菌内生孢子[16],可以保护其物种免受外部环境的干扰,为“仿生纳米平台”的发展提供了蓝图。特别是作为益生菌孢子的内在结构,孢子衣壳(spore capsid, SC)整合了许多独特的生物学特性,如抗性高、稳定性好等[17,18,19]。,可考虑用于口腔仿生孢子系统的构建。然而,SC在孢子萌发过程中会在肠道内分解,不能有效地用作口服药物的载体[20]。因此,基于简单高效的分离方法对SC进行合理的资本化,对于“仿生孢子纳米平台”的开发至关重要。在这项研究中,我们发现SC含有多种蛋白质,这些蛋白质赋予了它一些独特的生物活性,如“粘液惰性”性质和多受体介导的内吞作用。这些有希望的特性将为寻找口服给药的替代解决方案提供线索。
此外,联合化疗仍被认为是结肠癌临床治疗的主要策略,因为它可以克服肿瘤细胞的耐药和异质性问题[21,22,23,24]。正如我们之前报道的那样,化疗药物(盐酸阿霉素,DOX)和分子靶向药物(索拉非尼,SOR)可以作为协同治疗药物来增强结肠癌的治疗效果[25]。虽然这种协同策略很有前景,但如何克服这两种游离药物固有的局限性,如水溶性差[26]、血液清除率快[27]和生物利用度低[28],仍然是一个很大的挑战。有趣的是,具有π共轭结构和大量羟基的DOX可以与SOR形成稳定的氢键。因此,我们有理由推测DOX和SOR可以通过氢键和π-π堆叠相互作用自组装形成无载流子NPs (DOX/SOR NPs, DS NPs)[29,30]。不幸的是,DS NPs不能抵抗恶劣的胃环境,它们的使用通常受到全身药物暴露引起的副作用的限制。
因此,受益生菌孢子中观察到的SC的这些独特特征的启发,我们首先使用原始方法分离了总SC,并通过质谱分析确定了其蛋白质种类。然后,基于SC,开发了一种新型的多功能集成仿生孢子纳米平台(SC@DS NPs),以一站式解决上述问题(方案1)。在该系统中,首先通过自组装制备DOX和SOR作为DS NPs,然后涂覆从益生菌孢子中分离出来的SC。结果表明SC@DS NPs可以顺利通过复杂的胃环境,这与SC的保护性递送有关。此外,SC富含半胱氨酸,含有大量巯基,可以裂解粘液糖蛋白之间的二硫键,从而具有良好的逃避粘液陷阱的效果。令人惊讶的是,我们发现SC@DS NPs具有显著的跨上皮运输效率,这与SC的蛋白质种类有关。我们证明了这种仿生孢子纳米平台可以先后克服粘膜扩散屏障和上皮吸收屏障。我们的工作提供了一个简单、安全的仿生纳米平台,可能有助于指导口服NPs给药系统的开发。
方案1
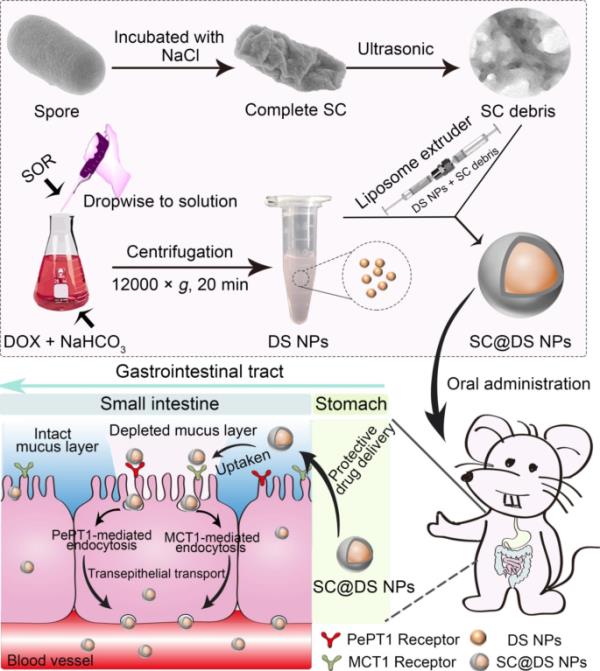
仿生孢子纳米平台的制备及口服递送机制示意图
首先,利用扫描电镜(SEM)和透射电镜(TEM)对菌体和孢子形态进行了表征。可以看到,粒径为3 ~ 5 μm的BC呈棒状(附加文件1:图S1),而粒径为1 ~ 2 μm的孢子则成功从BC中分离出来,孢子呈饱满完整的形状(图1a)。此外,Gram菌株也证实了BC的成功培养和孢子的分离(附加文件1:图S2)。随后,将BC孢子用不同浓度的氯化钠(NaCl)溶液孵育,制备孢子衣壳(SC)。与在盐水中分散的孢子表面光滑(图1a)相比,在5% NaCl中培养2 h后,孢子表面出现轻微褶皱(附加文件1:图S3a),并且随着NaCl浓度的增加,孢子收缩程度增大(附加文件1:图S3b)。因此,在本研究中,将孢子分散在20%的NaCl中,得到纯净的SC。如图1b所示,孢子的形态收缩更为严重。此外,透射电镜图像显示,在红色箭头所指向的孢子中有明显的裂缝,这可能是导致主要内容物从孢子中释放出来的原因。这一现象表明SC从孢子中分离成功。鉴于SC对恶劣环境的高抗性[17],我们推测SC可以通过口服给药作为递送纳米颗粒(NPs)的载体。然后用超声波均质机对SC进行破碎,制备SC碎屑。如附加文件1:图S4所示,BC呈片层状结构,有利于NPs的制备和形成以及药物的装载。
图1
制备和表征。(a)孢子和(b) SC的SEM和TEM图像。(c) DS NPs和(d) SC@DS NPs的SEM和TEM图像。(e)在SGF中孵育2 h后观察DS NPs和SC@DS NPs的形态。(f) DS NPs和SC@DS NPs在SGF中的累积DOX和SOR释放。(g) SIF孵育4 h后DS NPs和SC@DS NPs的形态变化。(h)在SIF中孵育4 h后,DS NPs和SC@DS NPs组中SOR和DOX的累积释放量。(i)在pH逐渐变化的缓冲液中孵育24 h以上后,DS NPs和SC@DS NPs中药物的释放行为。(j) 37℃下不同制剂模拟黏液中形成的颗粒-粘蛋白聚集百分比
此外,可以采用两药联合的策略来提高治疗效果[31,32,33]。因此,作为概念验证,我们选择水溶性DOX和疏水性SOR通过纳米沉淀法形成DS NPs[30]。令人惊讶的是,如图1c和附加文件1:图S5所示,DS NPs具有良好的形态和良好的分散性。DS NPs在266 nm处(红色箭头)和480 nm处(黑色箭头)的紫外吸收峰分别与游离SOR和DOX的最大吸收峰一致,进一步证明了DS NPs的成分为DOX和SOR(附加文件1:图S6)。随后,如图1d和附加文件1:Table S1所示,与DS NPs相比,SC@DS NPs的表面有较厚的涂层,这证实了SC@DS NPs经过13次挤压后成功合成。此外,与未涂覆的DS NPs相比,SC在DS NPs表面的有效包裹进一步证明了粒径的轻微增加和表面电荷的变化(附加文件1:图S7和S8)。值得注意的是,SC@DS NPs的蛋白质组成与SC相似,这表明SC涂层过程几乎不会影响SC的表面组成(附加文件1:图S9)。随着室温下储存时间的延长,粒径和zeta电位的变化可以忽略不计,这说明SC@DS NPs具有优越的稳定性(附加文件1:图S10和S11)。此外,还评估了SC@DS NPs在PBS、血清和细胞培养基中的稳定性。如附加文件1:Fig. S12所示,SC@DS NPs在各种生物介质中分散良好,具有良好的生物相容性和生物稳定性。
考虑到孢子外壳是孢子抵抗恶劣酸性环境的关键因素,我们推测SC在胃中相对稳定。为了研究SC是否对DS NPs具有保护作用,我们将DS NPs和SC@DS NPs分别置于模拟胃液(SGF)中孵育。孵育2 h后,用透射电镜观察其形态。如图1e所示,DS NPs被破坏,而SC@DS NPs可以保持完整的形状,这表明SC可以作为保护载体。此外,在SGF中孵育期间,还评估了DOX和SOR的药物释放情况。从图1f可以看出,DOX和SOR在DS NPs中的释放量接近100%。而SC@DS NPs的释放量可忽略不计,进一步证实了SC的保护作用。此外,将DS NPs和SC@DS NPs分别在受激肠液(SIF)中孵育4 h后,对两种NPs的药物释放特性和形态变化进行了评价。如图1g所示,大多数DS NPs断裂(红色箭头),不能保持完整的形态。虽然SC@DS NPs可以保持良好的形状,但由于肠道特异性酶的存在,仍有一些轻微的损伤,这可能导致SIF中药物释放率较低,约为30%(图1)。将DS NPs和SC@DS NPs在SIF中预孵育4 h后,转移到pH 7.4和pH 5.5的溶液中孵育。如图1i所示,DS NPs在pH 7.4和pH 5.5下均有较高的释放率。而SC@DS NPs在pH 7.4中孵育20 h后几乎没有药物释放,而转移到pH 5.5溶液中则有持续的药物释放。这一结果表明SC@DS NPs可以在肿瘤微环境中实现持续的药物释放。
值得注意的是,粘液屏障可降低肠上皮对NPs的吸收效率[34]。我们进一步用LCMSMS (nanoLC-QE)分析了SC的特异性蛋白质成分。如附加文件1:表S2所示,SC中含有大量的半胱氨酸,这可能导致SC粘液的高渗透性。众所周知,粘液是由复杂的生化成分组成的,它可以吸附包括药物在内的各种分子和颗粒,以及其他潜在的有害物质[35,36]。如图1j所示,D/S处理组检测到较高的聚集率,这是因为小分子药物可以被肠道粘液捕获并快速移除。其中SC@DS NPs的聚集率较低,为7.2%±4.7%,这可以解释为含有半胱氨酸的SC可以切割黏液糖蛋白之间的二硫键,增加DS NPs在肠道黏液中的渗透性[37,38]。此外,通过共聚焦激光扫描显微镜(CLSM)进行z轴扫描,观察细胞单层上NPs(红色)的垂直分布(附加文件1:图S13)。DOX和DS NPs处理组的荧光信号与黏液层有较强的相关性,而SC@DS NPs的荧光信号很少覆盖在黏液上,说明很大一部分SC@DS NPs能够逃脱黏液的捕获。此外,我们接下来研究了这些差异是否归因于粘膜表面NPs的诱捕或通透性的改变。在SC@DS NPs中观察到红色和绿色荧光的明显分离,表明其具有优异的逃避粘液捕获的能力和良好的渗透性(附加文件1:图S14)。
有效的上皮摄取和经上皮转运对口服NPs递送起着至关重要的作用[39]。首先,分别评价SC和SC@DS NPs对Caco-2细胞的细胞毒性。当SC和SC@DS NPs浓度达到500μg/mL时,细胞存活率约为95%,表明该药物载体体系具有良好的生物相容性,对Caco-2细胞无明显毒性(附加文件1:图S15)。值得注意的是,我们发现与其他处理组相比,SC@NPs显著提高了Caco-2细胞的细胞摄取率(图2a, b和附加文件1:图S16)。这是因为SC中含有一些能与上皮受体结合的靶蛋白。被这一有希望的结果所吸引,我们进一步研究了SC@DS NPs的内吞作用机制。如图2c所示,阿米洛利和M-β-CD分别作为巨噬细胞非特异性抑制剂和脂质筏干扰物通路抑制剂,可以显著降低DS NPs处理组的细胞摄取。此外,氯丙嗪和洛伐他汀分别是网格蛋白介导的内吞作用途径和小泡介导的内吞作用途径的抑制剂。有趣的是,SC@DS NPs分别用氯丙嗪(减少11%)和洛伐他汀(减少11.9%)处理后,显示出显著的细胞摄取抑制作用。这些结果表明SC@DS NPs的细胞摄取效率涉及多种细胞途径,如脂筏和小泡介导的摄取,网格蛋白依赖的内吞作用以及巨噬细胞作用。正如预期的那样,这种内吞途径的非特异性可能有助于提高它们的细胞摄取效率。
图2
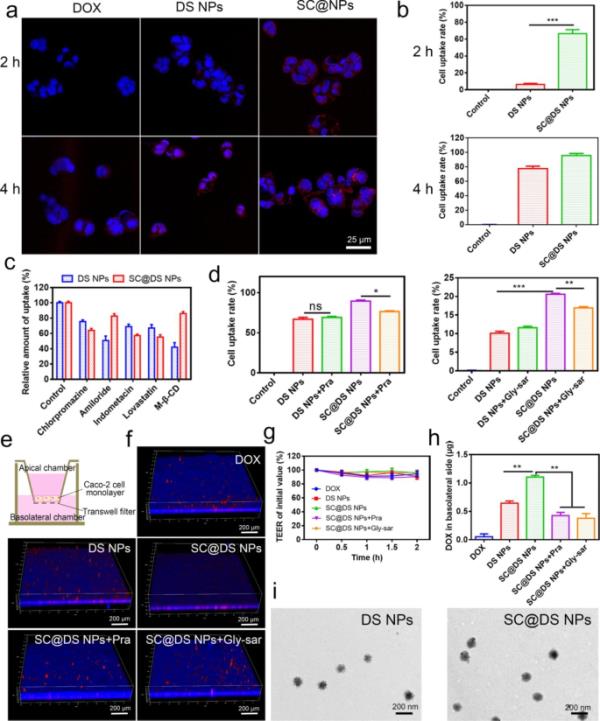
摄取机制及经上皮转运的研究。(a)细胞在孵育2和4 h时对游离DOX、DS NPs和SC@DS NPs的摄取。(b) Caco-2细胞分别与DS NPs和SC@DS NPs孵育2和4 h后的流式细胞术统计分析结果。(c)与不同的内吞抑制剂孵育后Caco-2细胞的相对摄取的测量。(d) Pra和Gly-sar分别对DS NPs和SC@DS NPs细胞摄取的影响。(e) Caco-2细胞单层模型的建立。(f) Caco-2细胞单层上不同NPs从根尖到基底外侧的CLSM图像。(g)不同孵育前后Caco-2细胞单层的TEER值。(h)各组大鼠基底外侧腔内经上皮转运量。(i)基底外侧腔DS NPs和SC@DS NPs的TEM图像
此外,我们还研究了与SC@DS NPs高摄取相关的特异性受体介导的内吞作用。先前的研究认为,单羧酸转运体-1 (MCT1)是运输短链脂肪酸(SCFA)的主要受体,如丁酸盐、乳酸盐和丙酸盐[40]。如图2d所示,被称为MCT1抑制剂的普伐他汀(Pra)明显抑制了SC@DS NPs的细胞摄取。这一结果积极支持MCT1在scfa功能化纳米载体的内吞作用中发挥重要作用。此外,SC@DS NPs组摄取速率的增加可能与其他途径的额外激活有关。据报道,SC中含有一定量的酪氨酸,可能会增强寡肽转运体(PePT1)的受体介导的内吞作用[41]。glyyl -sarcos (Gly-Sar)作为PePT1受体的抑制剂,可以显著降低SC@DS NPs的摄取。在不与MCT1特异性相互作用的情况下,SC@DS NPs仍显示出较高的细胞摄取率。
随后,通过Caco-2细胞单层评估不同NPs的体外经上皮转运情况(图2e)。出乎我们意料的是,如图2f所示,SC@DS NPs处理组的荧光嵌入到细胞单层中,穿透到单层的基侧。而其他基团的荧光则漂浮在单层上,几乎观察不到这些NPs的穿透现象。然而,当细胞单层分别与不同途径抑制剂孵育时,SC@DS NPs很难实现有效的跨上皮运输。这一结果可以解释为SC@DS NPs的转运效率可以通过受体介导的内吞作用而提高。此外,不同处理前后单层细胞的经上皮电阻(TEER)值几乎没有变化(图2g)。紧密连接蛋白出现在上皮细胞和顶细胞膜边缘,切片中Occludin的阳性表达用红色标记(附加文件1:图S17)。有趣的是,与对照组一致,SC@DS NPs组在细胞核周围观察到环状连续的红色荧光。然而,在其他处理组中检测到不连续的红色荧光。这些结果都证明SC@DS NPs的通透性是由受体介导的跨细胞转运引起的,而不是细胞单层完整性的破坏。基底侧室测量SC@DS NPs的跨细胞转运量,分别比Pra和Gly-sar预处理组高2.6倍和2.9倍(P < 0.05)(图2h)。同时,用透射电镜检测基底外侧腔内不同NPs的形态。如图2i所示,DS NPs边缘粗糙,而具有完整性的SC@DS NPs表面光滑,这表明SC@DS NPs在跨上皮运输时具有良好的稳定性。
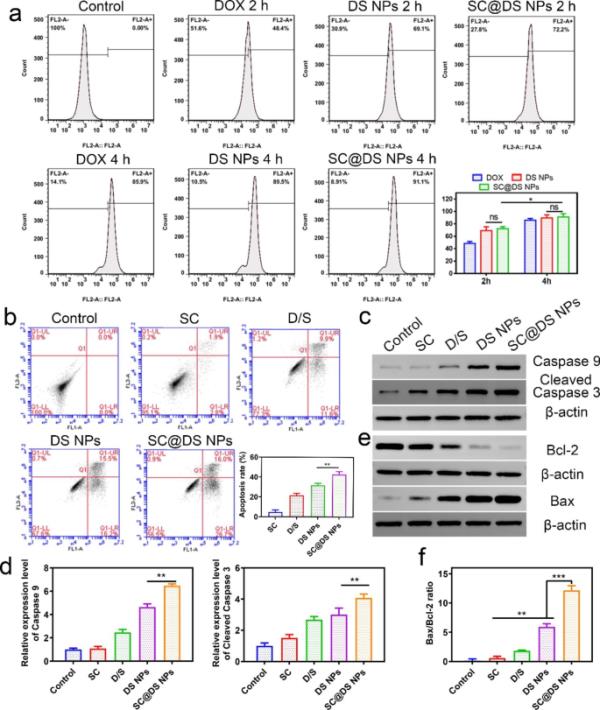
以人结肠肿瘤细胞系SW620为实验材料,考察其体外抗肿瘤效果。如图3a和附加文件1:Fig. S18所示,分别孵育2 h和4 h后,DS NPs和SC@DS NPs处理组之间无显著差异。提示SC仅通过特异性受体提高肠上皮运输效率,对肿瘤细胞没有明显的细胞摄取作用。然而,随着培养时间的延长,细胞对DS NPs和SC@DS NPs的摄取明显高于DOX。同时检测不同组SW620细胞的凋亡水平。如图3b所示,SC@DS NPs组凋亡细胞较多,凋亡率为42.7±3.0%,明显高于DS NPs处理组(21.7±2.2%)和D/S处理组(21.5±2.1%)。这一结果归因于SC也能诱导肿瘤细胞轻度凋亡。Western blotting检测细胞凋亡水平。如Fig. 3c, d和附加文件1:Fig. S19所示,与SC@DS NPs孵育后,凋亡蛋白如caspase-9和cleaved caspase-3明显改善,表明SC@DS NPs可诱导严重的细胞凋亡。此外,肿瘤细胞的凋亡水平还受抗凋亡蛋白bcl-2和凋亡蛋白bax的调控[42]。各组bcl-2和bax的表达及bcl-2/bax比值的半定量分析见图3e、f和附加文件1:图S20。SC@DS NPs处理组bax/bcl-2比值明显低于其他各组,说明该制剂可促进细胞凋亡进程。
图3

SW620肿瘤细胞的细胞摄取和凋亡分析。(a)分别在孵育2和4 h时定量测定游离DOX、DS NPs和SC@DS NPs的细胞摄取量。(b)分别用D/S、DS NPs、SC和SC@DS NPs处理SW620细胞后的凋亡水平。(c) SW620细胞的caspase-9和cleaved-caspase-3蛋白水平。(d)不同组的半定量分析。(e) bax/bcl-2比值分析
既往研究认为孢子表面的半胱氨酸巯基可以裂解粘蛋白糖蛋白之间的二硫键,提高NPs对肠道粘液的渗透能力[16]。如图4a和附图S21所示,DOX处理组荧光强度较低,说明DOX不能穿透粘液。对于DS NPs处理组,虽然检测到明显的荧光信号,但肠上皮细胞摄取与黏液层表现出很强的相关性,表明更大比例的DS NPs被困在黏液中。体外颗粒-粘蛋白聚集实验也证实了这一结果。相反,在肠绒毛中可以明显观察到较高的荧光强度,而很少有荧光信号覆盖在粘液上。此外,如图4b所示,不同处理肠道组织的3D图像也证明SC@DS NPs可以显著避免粘液捕获,提高肠上皮细胞的摄取效率。这种现象可以解释为SC的保护功能。
图4
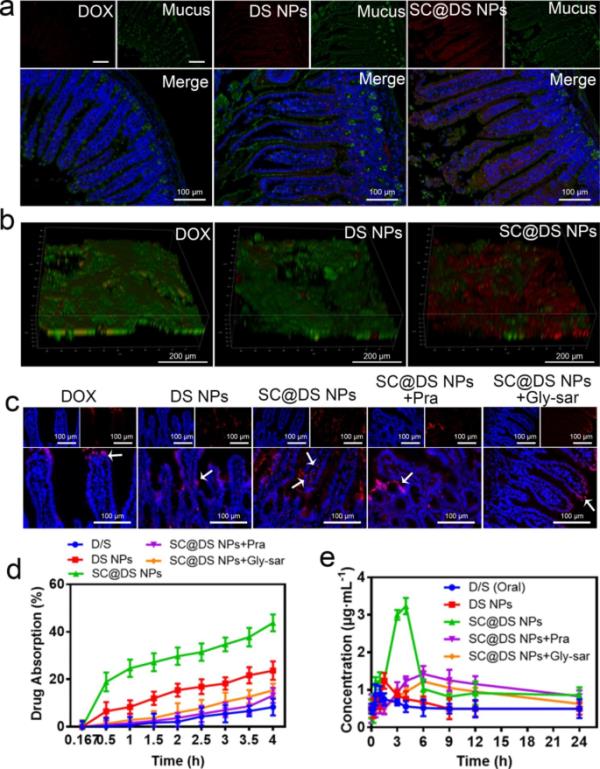
肠吸收和药代动力学参数的评价。(a)不同NPs的黏液渗透效果。(b)黏液中不同NPs分布的典型三维CLSM图像。(c)分别灌胃游离DOX、DS NPs、SC@DS NPs、SC@DS NPs + Pra和SC@DS NPs + Gly-sar后小鼠肠道代表性荧光图像。(d)原位肠循环吸收模型评价不同组大鼠肠道吸收情况。(e)口服剂量相当于30 mg kg - 1 DOX的不同组血浆药物浓度。
为了进一步研究不同NPs的体内肠道吸收情况,我们分别给小鼠口服游离DOX、DS NPs和SC@DS NPs 4 h。如图4c所示,小鼠经DS NPs处理后,在肠绒毛中检测到微弱的红色荧光信号,表明DS NPs吸收较差。正如预期的那样,SC@DS NPs治疗组上皮细胞和上皮基底外侧均观察到强烈的荧光信号。有趣的是,当SC@DS NPs处理组分别与Pra和Gly-sar预孵育时,它们在上皮细胞中表现出微弱的荧光信号。该结果表明SC@DS NPs在上皮细胞被有效吸收,并通过受体介导的内吞作用成功地转运到固有层。随后,通过体外结扎肠袢模型对原位肠道吸收和循环进行评价。如图4d所示,SC@DS NPs的药物吸收率为43.8%±3.5%,明显高于DS NPs的23.6%±3.9%。然而,当跨细胞途径被Pra或Gly-sar抑制时,SC@DS NPs的肠上皮吸收分别为13.2%±3.1%和15.4%±2.8%。上述结果提示SC@DS NPs可提高经上皮转运和吸收效率,这是提高治疗效果的重要前提。
鉴于SC@DS NPs具有良好的特性,我们进一步评估了D/S、DS NPs、SC@DS NPs、SC@DS NPs + Pra和SC@DS NPs + Gly-sar给药后的口服相对生物利用度。血药浓度时间曲线和药代动力学参数见图4e和附加文件1:表S3。DS NPs在1.5 h时的Cmax值为1.24±0.35μg mL?1,低于其他处理组。这一结果主要是由于DS NPs在通过恶劣的胃条件时稳定性差。值得注意的是,SC@DS NPs处理组的相对生物利用度(Frel)最高,比DS NPs处理组高5.6倍。此外,当用受体抑制剂对小鼠进行预处理,然后。
SC@DS NPs处理后,其相对生物利用度显著降低。综上所述,SC@DS NPs具有优异的黏液穿透和细胞摄取能力,可以作为一种有价值的药物传递系统,提高药物的生物利用度。
为了研究NPs的体内分布,采用近红外染料IR783代替DOX形成IR783 NPs自组装体。如图5a所示,游离IR783和IR783 NPs处理后,荧光信号在2 h时明显积聚到胃内。随着时间的延长,体内荧光分布明显下降。相比之下,SC@IR783 NPs处理小鼠后,肿瘤部位在8 h表现出强烈的荧光信号,直到12 h仍保持明显的荧光,而其他处理组的荧光信号几乎可以忽略。这种主要器官和肠道组织NPs实时分布的现象可以解释为:(i) SC可以保护NPs免受恶劣胃肠道环境的影响;(ii) SC可通过多种转运途径有效增强NPs的跨上皮转运能力,增加NPs进入血流的数量。这些有希望的NPs体内分布特征可能导致其具有较好的抗肿瘤功效。
图5
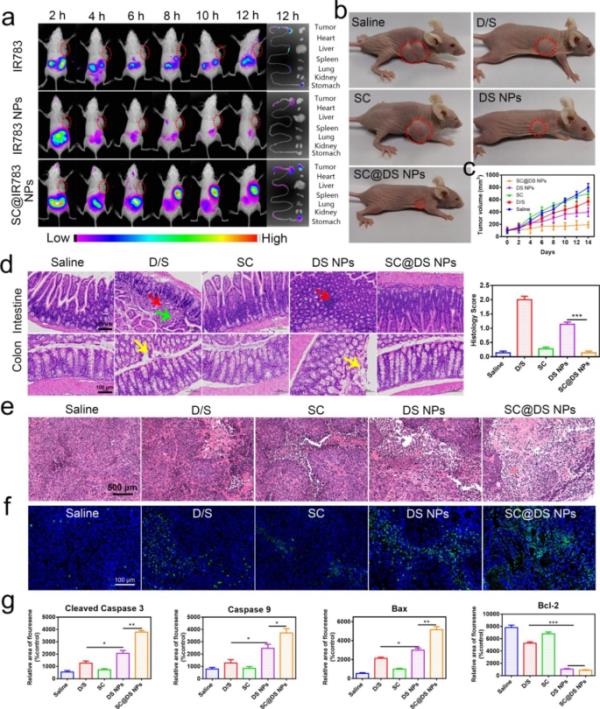
不同NPs的体内分布及治疗效果。(a)预设时间点SW620荷瘤小鼠体内成像。(b)不同处理后小鼠的代表性图片。(c)治疗期间肿瘤体积变化。(d)不同处理后肠、结直肠组织代表性H&E图像及组织学评分(红箭头:局灶性淋巴细胞浸润;黄箭头:上皮细胞脱屑,绿箭头:可见固有层结缔组织增生);标尺=100 μm。(e)不同处理肿瘤组织的H&E染色(比例尺=500 μm)。(f)各处理结束时肿瘤组织TUNEL染色(标尺=100 μm)。(g)不同处理细胞凋亡及抗凋亡相关蛋白裂解型caspase-3、caspase-9、bax、bcl-2的定量分析(mean±SD, n=6, *P < 0.05, **P < 0.01, ***P < 0.001)。不同的制剂分别以相当于30 mg kg - 1 DOX和5 mg kg - 1 SOR的剂量口服给鼠。采用多重比较的双向方差分析(ANOVA)或两组比较的t检验来评估显著差异
随后,分别用生理盐水、D/S、SC、DS NPs和SC@DS NPs治疗14天后,观察其体内肿瘤抑制效果。如附加文件1:图S22所示,由于DOX具有心脏毒性,D/S和SC处理组体重增加缓慢,而SC的治疗效果较弱。经SC@DS NPs处理的小鼠体重明显增加,说明SC@DS NPs具有良好的生物相容性和治疗效果。并记录每只小鼠的肿瘤体积,评价不同组的治疗效果。如图5b、c和附加文件1:图S23所示,生理盐水和SC治疗组均未观察到明显的肿瘤抑制作用。通过与D/S、DS NPs和SC@DS NPs治疗组的肿瘤体积比较,sc包被NPs对小鼠的抗肿瘤效果优于游离药组和NPs组。一旦将药物制备成NPs,再与SC进行功能化,肿瘤抑制效果就会提高。上述结果表明,具有良好生物安全性的SC可作为给药载体,对NPs具有良好的保护作用,可提高NPs在复杂GIT条件下的稳定性,提高抗肿瘤效果。
然后根据具体参数通过组织学评分变化评价小肠和结肠组织的病理特征(附加文件1:表S4)。如图5d所示,苏木精和伊红(H & E)测定表明,D/S和DS NPs可诱导局灶性淋巴细胞浸润等炎症反应;上皮细胞脱屑,固有层可见结缔组织增生。而SC@DS NPs治疗组未见明显炎症反应。此外,基于SC的组对主要器官的毒性几乎可以忽略不计(附加文件1:图S24),这表明SC@DS NPs具有优越的生物安全性。值得注意的是,AB-PAS染色(附加文件1:图S25)和MPO免疫荧光染色(附加文件1:图S26)进一步证明SC和SC基制剂不会引起肠细胞浸润和炎症,这与H&E染色结果一致。如图5e所示,生理盐水组和SC组肿瘤组织排列紧密,肿瘤细胞形态完整。相反,D/S和DS NPs组细胞核缩小,肿瘤细胞密度降低。有趣的是,在SC@DS NPs处理中检测到肿瘤细胞最显著的坏死,这证明SC可以阻止GIT条件下DS NPs的降解,提高体内抗肿瘤效果。为了进一步探讨不同治疗方法的治疗效果,我们采用TUNEL法评价肿瘤的凋亡特征。正如预期的那样,SC@DS NPs组显著观察到大量实质性的凋亡/坏死,这表明SC@DS NPs可以通过诱导凋亡途径抑制肿瘤的发展(图5f)。通过免疫荧光分析,肿瘤组织中凋亡或抗凋亡蛋白的表达也证实了这些抗肿瘤结果(图5g和附加文件1:图S27-30)。上述结果提示SC@DS NPs具有较好的抗肿瘤作用。
摘要
介绍
结果与讨论
结论
参考文献
致谢
作者信息
道德声明
搜索
导航
#####
综上所述,我们借鉴自然界中观察到的益生菌孢子的生物学特性,合理设计并开发了一种独特的仿生孢子纳米平台(SC@DS NPs),可以一次性克服粘膜扩散屏障和上皮吸收屏障。在该系统中,SC作为药物传递载体,具有多种功能。与DS NPs相比,SC@DS NPs保留了益生菌孢子的特性,口服后可抵抗极端胃酸环境,并成功递送至肠道。我们的研究表明,SC包被的NPs具有较低的黏蛋白亲和力和较好的黏液渗透能力。这一结果归因于SC富含巯基,可以裂解黏液糖蛋白之间的二硫键。我们发现SC@DS NPs的肠上皮吸收效率显著提高,因为SC含有一些特定的蛋白质。我们证明了这种仿生孢子纳米平台仅通过在NPs表面涂覆SC就可以先后克服粘膜扩散屏障和上皮吸收屏障。
以下是电子补充材料的链接。
下载原文档:https://link.springer.com/content/pdf/10.1186/s12951-023-01995-z.pdf
点击分享到









